Suvestinė redakcija nuo 2005-05-01 iki 2006-05-25
Įsakymas paskelbtas: Žin. 2004, Nr. 139-5076, i. k. 1042250ISAK000V-632
LIETUVOS RESPUBLIKOS SVEIKATOS APSAUGOS MINISTRO
Į S A K Y M A S
DĖL ŽMOGAUS KRAUJODAROS KAMIENINIŲ LĄSTELIŲ TRANSPLANTACIJOS PASLAUGŲ, APMOKAMŲ IŠ ŽMOGAUS ORGANŲ IR AUDINIŲ TRANSPLANTACIJOS PAPRASTŲJŲ IŠLAIDŲ FINANSAVIMO PROGRAMOS LĖŠŲ, TEIKIMO REIKALAVIMŲ, BAZINIŲ KAINŲ IR MOKĖJIMO TVARKOS APRAŠO PATVIRTINIMO
2004 m. rugsėjo 9 d. Nr. V-632
Vilnius
Tvirtinu Žmogaus kraujodaros kamieninių ląstelių transplantacijos paslaugų, apmokamų iš Žmogaus ir audinių transplantacijos paprastųjų išlaidų finansavimo programos lėšų, teikimo reikalavimus, bazines kainas ir mokėjimo tvarkos aprašą (pridedama).
PATVIRTINTA
Lietuvos Respublikos sveikatos apsaugos
ministro 2004 m. rugsėjo 9 d.
įsakymu Nr. V-632
ŽMOGAUS kraujodaros kamieninių ląstelių TRANSPLANTACIJOS PASLAUGŲ, APMOKAMŲ IŠ ŽMOGAUS ORGANŲ IR AUDINIŲ TRANSPLANTACIJOS PAPRASTŲJŲ IŠLAIDŲ FINANSAVIMO PROGRAMOS LĖŠŲ, teikimo reikalavimai, BAZINĖS KAINOS IR MOKĖJIMO TVARKOS Aprašas
I. Bendrosios nuostatos
1. Autologinė kraujodaros kamieninių ląstelių transplantacija (AUTOKKLT) – kraujodaros kamieninių ląstelių paėmimas ir persodinimas į to paties žmogaus kūną gydymo tikslu.
2. Alogeninė kraujodaros kamieninių ląstelių transplantacija (ALOKKLT) – kraujodaros kamieninių ląstelių paėmimas ir persodinimas į kito žmogaus kūną gydymo tikslu. Skiriamos šios ALOKKLT rūšys:
3. Kraujodaros kamieninių ląstelių šaltiniai:
4. Lietuvos negiminingų donorų registras (LNDR) yra Žmogaus audinių, ląstelių ir organų donorų bei recipientų registro sudėtinė dalis.
5. Sprendimas, ar atlikti kraujodaros kamieninių ląstelių transplantaciją, priimamas laikantis šių nuostatų:
5.1. Sprendimas, ar atlikti kraujodaros kamieninių ląstelių transplantaciją, priimamas individualiai, atsižvelgus į ligą, jos stadiją, prognozę, donoro buvimą bei tikimybę donorą rasti tinkamu laiku, bendrąją paciento būklę, organų funkciją bei kitus medicininius ir socialinius veiksnius.
5.2. Kraujodaros kamieninių ląstelių transplantacija gali būti atliekama tik pacientams, kurių būklė pagal Pasaulio sveikatos organizacijos bendrosios būklės rodiklį (PSO) 2 (1 priedas).
5.3. Sprendimą, ar atlikti kraujodaros kamieninių ląstelių transplantaciją, priima trijų kraujodaros kamieninių ląstelių transplantacijas atliekančių hematologų ar vaikų hematologų konsiliumas, kuriame dalyvauja hematologijos (onkohematologijos) padalinio vadovas. Sprendimas įrašomas Konsiliumo dėl indikacijų kraujodaros kamieninių ląstelių transplantacijai atlikti protokole (2 priedas). Šis protokolas saugomas kartu su pildomais medicinos dokumentais (ligonio gydymo stacionare ligos istorija Nr. 003/a ar asmens sveikatos istorija Nr. 025/a). Už konsiliumų šaukimą atsakingas kraujodaros kamieninių ląstelių transplantacijos padalinio vadovas.
6. Pacientų, kuriems bus atliekama kraujodaros kamieninių ląstelių transplantacija, sąrašo sudarymo principai:
6.1. Į Pacientų, kuriems bus atliekama kraujodaros kamieninių ląstelių transplantacija, sąrašą įtraukiami pacientai, kurie nurodyti gydytojų hematologų ar vaikų hematologų konsiliumo išvadose, pateiktose Konsiliumo dėl indikacijų kraujodaros kamieninių ląstelių transplantacijai atlikti protokole, ir kurie raštu sutinka, kad jiems būtų atlikta transplantacija (3 priedas). Vaikų iki 18 metų raštišką sutikimą pasirašo jų tėvai ar globėjai.
6.2. Iš Pacientų, kuriems bus atliekama kraujodaros kamieninių ląstelių transplantacija, sąrašo išregistruojami šie pacientai:
6.2.3. kuriems nustatytos nuolatinės kontraindikacijos transplantacijai atlikti, patvirtintos pakartotinio gydytojų hematologų ar vaikų hematologų konsiliumo;
6.3. Sprendimas išregistruoti pacientą iš sąrašo įrašomas Konsiliumo dėl indikacijų kraujodaros kamieninių ląstelių transplantacijai atlikti protokole (2 priedas). Šis protokolas saugomas kartu su pildomais medicinos dokumentais (ligonio gydymo stacionare ligos istorija Nr. 003/a ar asmens sveikatos istorija Nr. 025/a).
7. Skubos tvarka atliekama kraujodaros kamieninių ląstelių transplantacija:
7.1. Pacientui KKLT gali būti atliekama skubos tvarka, jei jam nustatytos skubios transplantacijos medicininės indikacijos.
7.2. Skubi transplantacija turi būti atliekama kuo skubiau, kai tik mediciniškai ir techniškai įmanoma.
7.3. Sprendimas transplantaciją atlikti skubos tvarka turi būti patvirtintas trijų kraujodaros kamieninių ląstelių transplantacijas atliekančių gydytojų hematologų ar vaikų hematologų konsiliumo, kuriame dalyvauja hematologijos (onkohematologijos) padalinio vadovas. Konsiliumo išvados įrašomos Konsiliumo dėl indikacijų kraujodaros kamieninių ląstelių transplantacijai atlikti protokole (2 priedas). Šis protokolas saugomas kartu su pildomais medicinos dokumentais (ligonio gydymo stacionare ligos istorija Nr. 003/a ar asmens sveikatos istorija Nr. 025/a). Už konsiliumų šaukimą atsakingas kraujodaros kamieninių ląstelių transplantacijos padalinio vadovas.
II. ŽMOGAUS kraujodaros kamieninių ląstelių TRANSPLANTACIJOS PASLAUGŲ TEIKIMO REIKALAVIMAI
8. Asmens sveikatos priežiūros įstaiga (toliau – įstaiga), kurioje atliekama kraujodaros kamieninių ląstelių transplantacija, turi atitikti bendruosius vidaus ligų profilio subspecializuotų stacionarinių tretinio lygio paslaugų teikimo reikalavimus bei teikti tretinio lygio hematologijos ir (ar) vaikų onkohematologijos paslaugas. Įstaiga, kurioje ketinama įdiegti kraujodaros kamieninių ląstelių transplantacijos paslaugas, turi pateikti Sveikatos apsaugos ministerijai duomenis ir gauti jos išvadą dėl šių paslaugų poreikio, investicijų, paprastųjų išlaidų pagrįstumo, veiklos efektyvumo bei kokybės.
9. Įstaigoje turi būti įrengtos mažiausiai 2 iš dalies izoliuotos vienvietės intensyviosios terapijos palatos, kuriose turi būti:
10. Įstaiga, kurioje atliekamos kraujodaros kamieninių ląstelių transplantacijos, privalo atitikti šiuos specialiuosius reikalavimus (pačioje įstaigoje ar kitose įstaigose, su kuriomis sudaryta sutartis):
10.1. Įstaigoje turi būti įrengta kraujodaros kamieninių ląstelių laboratorija, turinti kraujodaros kamieninių ląstelių manipuliacijų, programuojamo šaldymo bei ilgo laikymo įrangą.
10.2. Įstaigoje turi būti transfuziologijos padalinys, turintis ne mažiau kaip 2 ląstelių aferezės aparatus, kurie gali atlikti eritrocitaferezę, trombocitaferezę, leukaferezę, viso cirkuliuojančio plazmos tūrio pakeitimą (plazmaferezę), kraujodaros kamieninių ląstelių aferezę, limfocitaferezę, bei užtikrinantis:
10.2.1. visų kraujo komponentų parinkimą, pristatymą bei apšvitinimą ištisą parą. Padalinys privalo turėti kraujo komponentų apšvitos aparatą;
10.2.2. mažos leukocitų priemaišos trombocitų masės gamybą aferezės būdu; leukocitų priemaiša nustatoma imunocitometriškai. Padalinys privalo turėti ne mažiau kaip 2 ląstelių aferezės aparatus trombocitų masės gamybai. Jei įstaigoje atliekama daugiau kaip 30 kraujodaros kamieninių ląstelių transplantacijų per metus, ne mažiau kaip 80 proc. reikiamos trombocitų masės turi būti pagaminama pačioje įstaigoje.
11. Įstaigoje turi būti atliekami šie specialieji tyrimai (pačioje įstaigoje ar kitose įstaigose, su kuriomis sudaryta sutartis):
11.1. Tėkmės citometrijos tyrimai hemoblastozėms imunotipuoti, minimaliai liktinei ligai nustatyti, kraujodaros kamieninių ląstelių koncentracijai kraujyje ir aferezės produktuose nustatyti.
11.3. Infekcinių ligų molekulinės genetikos tyrimai: kiekybiniai citomegalijos ir Ebšteino Baro, hepatitų B ir C virusų, kokybiniai adenoviruso, respiracinio sincitinio, herpes simpleks I/II virusų bei pageidautini kitų sukėlėjų tyrimai.
12. Autologinės žmogaus kraujodaros kamieninių ląstelių transplantacijos paslaugų teikimo reikalavimai:
12.1. Įstaigos, kuri teikia autologinės kraujodaros kamieninių ląstelių transplantacijos paslaugas, specialieji reikalavimai:
12.1.1. įstaigoje AUTOKKLT gali būti atliekama tik po to, kai ne trumpiau kaip 5 metus buvo sistemingai taikoma didelių dozių chemoterapija onkohematologinėms ligoms gydyti;
12.2. Indikacijos atlikti autologinę kraujodaros kamieninių ląstelių transplantaciją:
| Diagnozė |
TLK-10 kodai |
Papildomos sąlygos |
| Ūmi mieloleukemija |
C92.0, C92.2-C92.7, C93.0, C93.2, C93.7, C93.9, C94.0, C94.2-C94.5 |
Pilna remisijaa |
| Ūmi limfoleukemija |
C91.0, C91.2-C91.7, C91.9 |
Pilna remisijaa |
| Ūmi bifenotipė leukemija, ūmi nepatikslinta leukemija |
C94.7, C95.0 |
Pilna remisijaa |
| Mielodisplazijos sindromas su blastų pertekliumi |
D46.2-D46.3 |
Pilna remisijaa |
| Lėtinė mieloleukemija |
C92.1 |
Lėtinė fazėb |
| Lėtinė limfoleukemija |
C91.1 |
Progresavimasc Remisija |
| Ne Hodžkino limfoma, piktybinės imunoproliferacinės ligos |
C82-C85, C88 |
Progresavimasd Atkrytise Pirminė liga, kai tarptautinis prognozės indeksas (IPI) > 1 (agresyvios, ne Hodžkino limfomos) |
| Hodžkino limfoma |
C81 |
Progresavimasd Atkrytis po chemoterapijose |
| Mielominė liga |
C90 |
Indikuotina |
| Histiocitozė ir hemofagocitiniai sindromai |
C96, D76 |
Piktybinė forma Progresavimasd Atkrytise |
| Germinogeniniai navikai |
C37, C56, C62, C73 |
Didelės rizikos pirminiai navikaif Progresavimasd Atkrytise |
| Ewingo sarkoma, PNET |
C00-C06, C30, C31, C38, C40, C41, C47-C49, C69, C74 |
Didelės rizikos pirminiai navikaig Progresavimasd Atkrytise |
| Neuroblastoma |
C00-C06, C30, C31, C38, C40, C41, C47-C49, C69, C74 |
Didelės rizikos pirminiai navikaih Atkrytise |
PASTABOS:
a – Mažiau kaip 5 proc. leukemijos blastų kaulų čiulpuose.
b – Mažiau kaip 10 proc. leukemijos blastų periferiniame kraujyje ar kaulų čiulpuose, mažiau kaip 20 proc. leukemijos blastų ir promielocitų kraujyje ar kaulų čiulpuose.
c – Bent vienas iš požymių: limfocitozės, limfmazgių, organų didėjimas, progresuojanti anemija, neutropenija, trombocitopenija.
d – Bent vienas iš požymių: išliekantys sisteminiai ligos simptomai, naujų ligos požymių atsiradimas, mažesnė kaip 50 proc. regresija.
e – Ligos atsinaujinimas po pilnos ar dalinės remisijos.
f – Ne seminoma ir bent vienas iš požymių: pirminis tarpuplaučio navikas, ne plaučių metastazės, AFP > 10 000 ng/ml, hCG > 50 000 IU/ml, LDH > 10 kartų didesnė už viršutinę normos ribą.
g – Bent vienas iš požymių: metastazės, naviko nekrozė po indukcinės chemoterapijos < 90 proc., pirminio naviko tūris > 200 ml ir neįvertinama naviko nekrozė po chemoterapijos, aksialinis navikas.
h – Bent vienas iš požymių: IV stadija, I–III stadija ir MYCN amplifikacija, blogas atsakas į standartinę chemoterapiją.
12.3. Autologinę kraujodaros kamieninių ląstelių transplantaciją sudaro:
12.3.1. potencialaus recipiento sutikimas, kad jam būtų atlikta autologinė kraujodaros kamieninių ląstelių transplantacija (3 priedas);
12.3.3. kraujodaros kamieninių ląstelių mobilizacija granulocitų kolonijas stimuliuojančiu veiksniu ir (ar) citostatikais, surinkimas, užšaldymas ir laikymas;
12.3.4. recipiento kondicionavimas, kraujodaros kamieninių ląstelių infuzija į recipiento veną, pradinis laikotarpis po AUTOKKLT, kai būtina hospitalizuoti recipientą;
12.4. Pagrindiniai vaistai ir vienkartinės priemonės, naudojami AUTOKKLT metu:
12.4.11. vienkartinės sistemos: trombocitaferezės, leukocitaferezės, plazmaferezės, kaulų čiulpų separacijos, kaulų čiulpų surinkimo, kaulų čiulpų filtravimo, parenterinio maitinimo;
13. Alogeninės kraujodaros kamieninių ląstelių transplantacijos paslaugų teikimo reikalavimai:
13.1. Įstaigos, kuri teikia alogeninės kraujodaros kamieninių ląstelių transplantacijos paslaugas, specialieji reikalavimai:
13.1.1. įstaigoje giminingo donoro ALOKKLT gali būti atliekamos tik po to, kai ne trumpiau kaip 5 metus buvo atliekama AUTOKKLT ir atlikta ne mažiau kaip 60 AUTOKKLT (PASTABA. Ši nuostata netaikoma įstaigoms, kurios pradėjo ALOKKLT prieš įsigaliojant šiam įsakymui);
13.1.2. įstaigoje negiminingo donoro ALOKKLT gali būti atliekamos tik po to, kai ne trumpiau kaip 5 metus buvo atliekama giminingo donoro ALOKKLT ir atlikta ne mažiau kaip 40 ALOKKLT (PASTABA. Ši nuostata netaikoma įstaigoms, kurios pradėjo ALOKKLT prieš įsigaliojant šiam įsakymui);
13.1.3. įstaigoje turi dirbti ne mažiau kaip 2 gydytojai hematologai ar vaikų hematologai, turintys ne trumpesnį kaip 2 metų ALOKKLT atlikimo stažą.
13.1.4. Įstaiga privalo turėti šias laboratorijas ir atlikti tokius tyrimus (pačioje įstaigoje ar kitose įstaigose, su kuriomis sudaroma sutartis):
13.2. Indikacijos atlikti alogeninę kraujodaros kamieninių ląstelių transplantaciją:
| Diagnozė |
TLK-10 kodai |
Papildomos sąlygos |
|
|
|
|
Gimininga |
Negimininga |
| Ūmi mieloleukemija |
C92.0, C92.2-C92.7, C93.0, |
Pilnaa ar dalinėb remisija |
Pilnaa ar dalinėb remisija |
|
|
C93.2, C93.7, C93.9, C94.0, |
Prasidedantis atkrytisc |
Prasidedantis atkrytisc |
|
|
C94.2-C94.5 |
|
|
| Ūmi limfoleukemija |
C91.0, C91.2-C91.7, C91.9 |
Pilnaa ar dalinėb remisija |
Pilnaa ar dalinėb remisija |
|
|
|
Prasidedantis atkrytisc |
Prasidedantis atkrytisc |
| Ūmi bifenotipė leukemija, ūmi |
C94.7, C95.0 |
Pilnaa ar dalinėb remisija |
Pilnaa ar dalinėb remisija |
| nepatikslinta leukemija |
|
Prasidedantis atkrytisc |
Prasidedantis atkrytisc |
| Mielodisplazijos sindromas |
D46, C93.1 |
Indikuotina |
Indikuotina |
| Lėtinė mieloleukemija |
C92.1 |
Lėtinėd ar akceleracijose stadija |
Lėtinėd ar akceleracijose stadija |
| Lėtinė mieloproliferacinė liga |
D47.1 |
Progresavimasf |
Progresavimasf |
| Lėtinė limfoleukemija |
C91.1 |
Progresavimasg |
Progresavimasg |
|
|
|
Remisija |
Remisija |
| Ne Hodžkino limfoma, piktybinės |
C82-C85, C88 |
Progresavimash |
Progresavimash |
| imunoproliferacinės ligos |
|
Atkrytisi |
Atkrytisi |
| Hodžkino limfoma |
C81 |
Progresavimash |
Progresavimash |
|
|
|
Atkrytisi |
Atkrytisi |
| Mielominė liga |
C90 |
Indikuotina |
Neindikuotina |
| Aplazinė anemija, eritropoezės aplazija |
D60, D61 |
Indikuotina |
Indikuotina |
| Talasemija |
D56 |
Sunkios formos |
Sunkios formos |
| Histiocitozė ir hemofagocitiniai sindromai |
C96, D76 |
Piktybinė forma |
Piktybinė forma |
|
|
|
Progresavimash |
Progresavimash |
|
|
|
Atkrytisi |
Atkrytisi |
| Germinogeniniai navikai |
C37, C56, C62, C73 |
Kai indikuotina AUTOKKLT, |
Neindikuotina |
|
|
|
tačiau dėl techninių kliūčių jos |
|
|
|
|
atlikti neįmanoma |
|
| Ewingo sarkoma, PNET |
C00-C06, C30, C31, C38, |
Kai indikuotina AUTOKKLT, |
Neindikuotina |
|
|
C40, C41, C47-C49, C69, C74 |
tačiau dėl techninių kliūčių jos |
|
|
|
|
atlikti neįmanoma |
|
| Įgimti kraujodaros, medžiagų apykaitos |
D64, D69.4, D70, D71, D81, |
Sunkios formos |
Sunkios formos |
| sutrikimai, imunodeficitai (įgimta diseritropoezinė anemija, įgimta amegakariocitinė trombocitopenija, trombocitopenija su nesančiu stipinkauliu, agranulocitozė, kombinuotas imunodeficitas, kiti imunodeficitai, Wiskotto-Aldricho sindromas, medžiagų apykaitos sutrikimai su kraujodaros sistemos pažeidimu, adrenoleukodistrofija) |
D82, E71, E75-E77, Q87 |
|
|
PASTABOS:
a – Mažiau kaip 5 proc. leukemijos blastų kaulų čiulpuose.
b – 6–20 proc. leukemijos blastų kaulų čiulpuose.
c – Pogresuojanti neutropenija, anemija, trombocitopenija ir mažiau kaip 5 proc. leukemijos blastų kaulų čiulpuose.
d – Mažiau kaip 10 proc. leukemijos blastų periferiniame kraujyje ar kaulų čiulpuose, mažiau kaip 20 proc. leukemijos blastų ir promielocitų kraujyje ar kaulų čiulpuose.
e – Leukemijos blastų kaulų čiulpuose yra 10–19 proc., leukemijos blastų ir promielocitų kraujyje ar kaulų čiulpuose – 20–29 proc.
f – Bent vienas iš požymių: leukocitozės, organų didėjimas, progresuojanti anemija, neutropenija, trombocitopenija.
g – Bent vienas iš požymių: limfocitozės, limfmazgių, organų didėjimas, progresuojanti anemija, neutropenija, trombocitopenija.
h – Bent vienas iš požymių: išliekantys sisteminiai ligos simptomai, naujų ligos požymių atsiradimas, mažesnė kaip 50 proc. regresija.
i – Ligos atsinaujinimas po pilnos ar dalinės remisijos.
13.3. Alogeninę kraujodaros kamieninių ląstelių transplantaciją sudaro:
13.3.1. potencialaus donoro sutikimas, kad jo kraujodaros kamieninės ląstelės būtų panaudotos transplantacijai (4 priedas);
13.3.5. gimininga ALOKKLT: giminingo donoro kraujodaros kamieninių ląstelių mobilizacija granulocitų kolonijas stimuliuojančiu veiksniu bei kamieninių ląstelių surinkimas ląstelių aferezės aparatu arba iš kaulų čiulpų;
13.3.6. negimininga ALOKKLT: donoro paieška LNDR ar Pasaulio negiminingų donorų registre, jo kvietimas ir ištyrimas, kraujodaros kamieninių ląstelių surinkimas bei atvežimas;
13.3.7. recipiento kondicionavimas, donoro kraujodaros kamieninių ląstelių infuzija į recipiento veną, pradinis laikotarpis po ALOKKLT, kai reikia hospitalizuoti recipientą;
13.4. Pagrindiniai vaistai ir vienkartinės priemonės:
13.4.11. vienkartinės sistemos: trombocitaferezės, leukocitaferezės, plazmaferezės, kaulų čiulpų separacijos, kaulų čiulpų surinkimo, kaulų čiulpų filtravimo, parenterinio maitinimo;
III. alogeninių negiminingų donorų kaulų čiulpų transplantacijų koordinavimas ir Negiminingų donorų paieška
14. Įstaigos, kuri teikia negiminingų donorų ALOKKLT koordinavimo paslaugas, specialieji reikalavimai:
14.1. įstaigoje turi būti hematologijos padalinys, kuris ne trumpiau kaip 5 metus atlieka giminingą ALOKKLT ir per šį periodą yra atlikęs ne mažiau kaip 40 ALOKKLT;
14.3. turi būti įrengta klinikinės imunologijos laboratorija, atliekanti:
15. Negiminingų donorų ALOKKLT koordinavimo paslaugas teikianti įstaiga:
15.1. skiria ne mažiau kaip trijų gydytojų negiminingų donorų ALOKKLT priežiūros komisiją, kurią sudaro hematologijos bei transplantacijos padalinių vadovai gydytojai hematologai ir gydytojas klinikinis imunologas, atliekantis audinių suderinamumo tyrimus, ir kuri:
15.1.2. nustato negiminingo donoro paieškos strategiją, atsižvelgdama į ŽLA tapatumą, rasę, amžių, lytį, kraujo grupę, infekuotumą citomegalijos virusu, negiminingo donoro paieškos, jo kvietimo ir ištyrimo, bei kamieninių ląstelių surinkimo išlaidas;
15.2. skiria koordinatorių, kuris tvarko dokumentus, atlieka negiminingo donoro paiešką bei gabena kraujodaros kamienines ląsteles;
16. Negiminingų donorų atranka į Lietuvos negiminingų donorų registrą:
16.1. negiminingais kraujodaros kamieninių ląstelių donorais gali būti ne jaunesni kaip 18 metų ir ne vyresni kaip 55 metų asmenys savanoriai;
16.2. kontraindikacijos įtraukti į negiminingų kraujodaros kamieninių ląstelių donorų registrą:
16.2.1. potencialaus donoro priklausymas didelės rizikos grupei: narkomanija, prostitucija, alkoholizmas;
17. Potencialaus negiminingo donoro įrašymo į Lietuvos negiminingų donorų registrą tvarka:
17.1. Asmuo, norintis tapti negiminingu kraujodaros kamieninių ląstelių donoru, kreipiasi į kraujo donorystės įstaigą, kuri organizuoja jo ištyrimą (6 priedas).
17.2. Asmuo, kuris nori būti įregistruotas negiminingu kraujodaros kamieninių ląstelių potencialiu donoru, užpildo Negiminingo kraujo kamieninių ląstelių potencialaus donoro anketą (7 priedas) bei Savanorio negiminingo kraujo kamieninių ląstelių donoro sutikimą įtraukti duomenis į LNDR duomenų bazę (8 priedas). Pasirašydamas donoro anketą, asmuo patvirtina, kad jam buvo pateikti šios anketos klausimai ir atsako už informacijos teisingumą.
17.3. Jei nėra klinikinių bei laboratorinių kontraindikacijų potencialų donorą registruoti LNDR, kraujo donorystės įstaiga potencialaus donoro kraujo mėginius, anketos, sutikimo originalus bei 17.1 skirsnyje numatytus tyrimų rezultatus siunčia į negiminingų ALOKKLT koordinavimo paslaugas teikiančią įstaigą.
17.4. Negiminingų ALOKKLT koordinavimo paslaugas teikianti įstaiga organizuoja šių tyrimų atlikimą:
17.4.1. ŽLA I klasės antigenų (ŽLA – A, B, C) nustatymo tyrimą limfocitotoksiniu ar molekulinės biologijos metodu;
IV. MOKĖJIMO UŽ ŽMOGAUS kraujodaros kamieninių ląstelių TRANSPLANTACIJOS PASLAUGAS TVARKOS APRAŠAS
18. Už žmogaus kraujodaros kamieninių ląstelių transplantacijų paslaugas mokama iš Privalomojo sveikatos draudimo fondo biudžeto lėšų, skirtų Žmogaus organų ir audinių transplantacijų programos paprastosioms išlaidoms finansuoti, neviršijant Privalomojo sveikatos draudimo fondo biudžeto skirtų asignavimų. Išlaidos, susijusios su negiminingo donoro tyrimu, numatytu 17.1 skirsnyje, apmokamos iš Privalomojo sveikatos draudimo fondo biudžeto lėšų, skirtų Žmogaus organų ir audinių transplantacijų programos paprastosioms išlaidoms finansuoti, tik tada, kai potencialus donoras nėra kartu ir kraujo ar jo komponentų donoras.
19. Asmens sveikatos priežiūros įstaiga, kurios gydytojų konsiliumas priėmė sprendimą dėl transplantacijos atlikimo tikslingumo ir ją organizavo užsienyje, apmoka transplantaciją atlikusiai asmens sveikatos priežiūros įstaigai pagal faktines išlaidas, neviršydama jai skirtų asignavimų.
20. Už naujai įdiegiamas žmogaus kraujodaros kamieninių ląstelių transplantacijos paslaugas atitinkama TLK viešajai asmens sveikatos priežiūros įstaigai moka iš Privalomojo sveikatos draudimo fondo biudžeto lėšų tik tada, kai Valstybinė medicininio audito inspekcija atlieka šių paslaugų medicininį auditą ir pateikia teigiamas išvadas.
21. Viešosios asmens sveikatos priežiūros įstaigos, teikiančios žmogaus kraujodaros kamieninių ląstelių transplantacijos paslaugas, pasibaigus ataskaitiniam mėnesiui, iki kito mėnesio 10 d. pateikia TLK suteiktų transplantacijos paslaugų ataskaitą VLK nustatyta tvarka.
22. Viešajai sveikatos priežiūros įstaigai skirtos lėšos Žmogaus organų ir audinių transplantacijos programai finansuoti apskaitomos banko įstaigos atskiroje sąskaitoje.
23. Viešosios asmens sveikatos priežiūros įstaigos sudaro ir patvirtina žmogaus kraujodaros kamieninių ląstelių transplantacijos išlaidų sąmatą pagal Finansų ministerijos nustatytą išlaidų klasifikaciją ir tvarko išlaidų apskaitą pagal galiojančią įstaigos išlaidų sąmatos struktūrą. Pasibaigus kiekvienam metų ketvirčiui, iki kito ketvirčio 15 d. viešosios asmens sveikatos priežiūros įstaigos pateikia TLK Biudžeto išlaidų sąmatos vykdymo apyskaitą (2 forma).
V. ŽMOGAUS KRAUJODAROS KAMIENINIŲ
LĄSTELIŲ TRANSPLANTACIJOS PASLAUGŲ BAZINĖS KAINOS
25. Autologinė kraujodaros kamieninių ląstelių transplantacija
| Transplantacijos etapai |
I etapas Kamieninių ląstelių mobilizacijos, surinkimo (stacionare), užšaldymo ir laikymo išlaidos |
II etapas Pirmųjų 45 dienų AUTOKKLT išlaidos (stacionare): recipiento kondicionavimas, kraujodaros kamieninių ląstelių infuzija į recipiento veną, pradinis laikotarpis po AUTOKKLT, kai būtina hospitalizuoti recipientą |
III etapas AUTOKKLT išlaidos (ambulatoriškai) |
IV etapas Vėlyvųjų komplikacijų po AUTOKKLT, dėl kurių būtina recipientą hospitalizuoti, gydymo išlaidos |
| Bazinė kaina suaugusiesiems (Lt) |
15578 |
74686 |
3960 |
75619 |
| Bazinė kaina vaikams iki 18 metų (Lt) |
12462 |
59749 |
3168 |
60495 |
PASTABA. III etapas tęsiamas ir tada, kai pacientas hospitalizuojamas dėl su AUTOKKLT nesusijusių priežasčių. Su AUTOKKLT susijusių gydymo ir tyrimų išlaidos apmokamos iš Žmogaus organų ir audinių transplantacijos paprastųjų išlaidų finansavimo programos lėšų.
26. Alogeninė kraujodaros kamieninių ląstelių transplantacija
| Transplantacijos etapai |
Ia etapas Donoro kraujodaros kamieninių ląstelių mobilizacijos bei surinkimo išlaidos Lietuvoje |
Ib etapasa Negiminingo donoro išlaidos |
II etapas Pirmųjų 100 dienų ALOKKLT išlaidos (stacionare): recipiento kondicionavimas, donoro kraujodaros kamieninių ląstelių infuzija į recipiento veną, pradinis laikotarpis po ALOKKLT, kai reikia hospitalizuoti recipientą |
III etapasb ALOKKLT išlaidos (ambulato-riškai) |
IV etapas Vėlyvųjų komplikacijų po ALOKKLT, dėl kurių būtina recipientą hospitalizuoti, gydymo išlaidos |
| Bazinė kaina suaugusiesiems (Lt) |
5154 |
Pagal faktines išlaidas, neviršijant 90000 |
216464 |
7171 |
116077 |
| Bazinė kaina vaikams iki 18 metų (Lt) |
5154 |
Pagal faktines išlaidas, neviršijant 90000 |
75763 |
7171 |
29020 |
PASTABOS:
a – Ib-1 Negiminingo donoro paieška LNDR ar Pasaulio negiminingų donorų registre, jo kvietimas ir ištyrimas.
Ib-2 Negiminingo donoro kraujodaros kamieninių ląstelių surinkimas užsienio šalyje.
Ib-3 Negiminingo donoro kraujodaros kamieninių ląstelių atvežimas iš užsienio šalies.
b – III etapas tęsiamas ir tada, kai pacientas hospitalizuojamas dėl su ALOKKLT nesusijusių priežasčių. Su ALOKKLT susijusių gydymo ir tyrimų išlaidos apmokamos iš Žmogaus organų ir audinių transplantacijos paprastųjų išlaidų finansavimo programos lėšų.
27. Vieno negiminingo donoro tyrimo, skirto Lietuvos negiminingų donorų registrui, išlaidos – 657 Lt
Skyriaus pakeitimai:
Nr. V-300, 2005-04-27, Žin., 2005, Nr. 55-1886 (2005-04-30), i. k. 1052250ISAK000V-300
Žmogaus kraujodaros kamieninių ląstelių
transplantacijos paslaugų, apmokamų iš
žmogaus organų ir audinių transplantacijos
paprastųjų išlaidų finansavimo programos
lėšų, teikimo reikalavimų, bazinių kainų ir
mokėjimo tvarkos aprašo
1 priedas

______________
Žmogaus kraujodaros kamieninių ląstelių
transplantacijos paslaugų, apmokamų iš
žmogaus organų ir audinių transplantacijos
paprastųjų išlaidų finansavimo programos
lėšų, teikimo reikalavimų, bazinių kainų ir
mokėjimo tvarkos aprašo
2 priedas
Konsiliumo dėl indikacijų kraujodaros kamieninių ląstelių transplantacijai atlikti protokolas
Data …………………
Pacientui (-ei) …………………………………………………….………………............................... ,
(vardas ir pavardė, asmens kodas)
sergančiam (-iai)..................................................... ................................................................................,
(diagnozė)
neindikuotina / indikuotina atlikti …..................................................................................................... ........................................................... ………………....................................………………………….
(transplantacijos pavadinimas)
planinę / skubią kraujodaros kamieninių ląstelių transplantaciją.
Paciento (-ės) bendroji būklė pagal PSO: ..............................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
Konsiliumo dalyviai
1.................................................. ............................................................................................................
(vardas ir pavardė) (parašas)
2................................................. .............................................................................................................
(vardas ir pavardė) (parašas)
3.............................................. ................................................................................................................
(vardas ir pavardė) (parašas)
......................................
(data)
Su konsiliumo išvadomis susipažinau:
.......................................................................................................................................... ......................
(paciento (tėvo ar globėjo) vardas ir pavardė) (parašas)
......................................
(data)
______________
Žmogaus kraujodaros kamieninių ląstelių
transplantacijos paslaugų, apmokamų iš
žmogaus organų ir audinių transplantacijos
paprastųjų išlaidų finansavimo programos
lėšų, teikimo reikalavimų, bazinių kainų ir
mokėjimo tvarkos aprašo
3 priedas
ASMENS SUTIKIMAS, KAD JAM BŪTŲ ATLIKTA KRAUJODAROS KAMIENINIŲ LĄSTELIŲ TRANSPLANTACIJa
Aš,...................................... ........................................................................................................,
(vardas ir pavardė, asmens kodas)
gimęs (-usi)....................................... ..........................................................................................,
gyvenantis (-i)..................................... .......................................................................................,
esu informuotas (-a) apie mano ligos pobūdį, ištyrimą ir gydymą, susipažinau su konsiliumo dėl indikacijų kraujodaros kamieninių ląstelių transplantacijai atlikti išvadomis. Man buvo išaiškinta ištyrimo ir gydymo rizika, galimos komplikacijos ir jų gydymo būdai.
Atlikus tyrimus buvo nustatyta, kad man reikalinga ši transplantacija.
Numatoma atlikti transplantacija:........................................... ....................................................
Transplantacijos metu atsiradus nenumatytoms aplinkybėms, sutinku, kad medicinos personalas imtųsi visų būtinų priemonių ir procedūrų, kurios, jo nuomone, toje situacijoje bus būtinos.
Susipažinau su kiekvienos procedūros rizikos veiksniais. Esu nurodęs (-iusi) visas savo ankstesnes ligas, kurios gali turėti įtakos tyrimui ir gydymui. Mane taip pat informavo apie kitus galimus (alternatyvius) tyrimo ir gydymo metodus, jų privalumus, trūkumus, komplikacijas ir gydymo sėkmę. Suprantu, kad medicinos praktikoje gali pasireikšti ir kitos, su manimi neaptartos komplikacijos. Esu informuotas (-a), kad ligoninėje yra visos priemonės ir galimybės komplikacijas diagnozuoti ir gydyti. Patvirtinu, kad man nebuvo duota jokių besąlyginių pažadų ar garantijų dėl teigiamo procedūros rezultato ar baigties.
Man buvo suteikta visa su mano būkle susijusi informacija ir atsakyta į visus man kilusius klausimus. Daugiau klausimų neturiu.
Visa tai apsvarstęs (-iusi), pareiškiu savo sutikimą atlikti kraujodaros kamieninių ląstelių transplantaciją.
Pacientas ………….........………… Gydytojas ………………………………
(parašas) (spaudas, parašas)
Paciento tėvas ar globėjas ……………………......................………………........................................
(vardas ir pavardė, asmens kodas) (parašas)
.......... m............................. mėn. ...... d.
______________
Žmogaus kraujodaros kamieninių ląstelių
transplantacijos paslaugų, apmokamų iš
žmogaus organų ir audinių transplantacijos
paprastųjų išlaidų finansavimo programos
lėšų, teikimo reikalavimų, bazinių kainų ir
mokėjimo tvarkos aprašo
4 priedas
asmens Sutikimas, kad jo kraujodaros kamieninės ląstelės būtų paimtos ir panaudotos transplantacijai
Aš,...................................... ........................................................................................................,
(vardas ir pavardė, asmens kodas)
gimęs (-usi)....................................... ..........................................................................................,
gyvenantis (-i)..................................... .......................................................................................,
esu informuotas (-a) apie kraujodaros kamieninių ląstelių paėmimo paskirtį, tikslus ir eigą. Man buvo išaiškinta šios procedūros rizika, galimos komplikacijos ir jų gydymo būdai.
Paėmimo metu atsiradus nenumatytoms aplinkybėms, sutinku, kad medicinos personalas imtųsi visų būtinų priemonių ir procedūrų, kurios, jo nuomone, toje situacijoje bus būtinos.
Man taip pat žinomas su kiekviena procedūra susijęs bendras rizikos veiksnys. Esu nurodęs (-džiusi) visas savo ankstesnes ligas, kurios gali turėti įtakos tyrimui ir gydymui.
Suprantu, kad medicinos praktikoje gali pasireikšti ir kitos, su manimi neaptartos komplikacijos. Esu informuotas (-a), kad ligoninėje yra visos priemonės ir galimybės komplikacijas diagnozuoti ir gydyti. Patvirtinu, kad man nebuvo duota jokių besąlyginių pažadų ar garantijų dėl teigiamo procedūros rezultato ar baigties.
Man buvo suteikta visa su mano būkle susijusi informacija ir atsakyta į visus man kilusius klausimus. Daugiau klausimų neturiu.
Visa tai apsvarstęs (-iusi), reiškiu savo sutikimą man atlikti kraujodaros kamieninių ląstelių donavimo procedūrą.
Donoras ………….........………… Gydytojas ………………………………
(parašas) (spaudas, parašas)
Donoras tėvas ar globėjas ……………………......................………………........................................
(vardas ir pavardė, asmens kodas) (parašas)
.......... m............................. mėn. ...... d.
______________
Žmogaus kraujodaros kamieninių ląstelių
transplantacijos paslaugų, apmokamų iš
žmogaus organų ir audinių transplantacijos
paprastųjų išlaidų finansavimo programos
lėšų, teikimo reikalavimų, bazinių kainų ir
mokėjimo tvarkos aprašo
5 priedas
DONORO ir (AR) recipiento IŠTYRIMas prieš kraujodaros kamieninių ląstelių transplantaciją
1. Klinikinis tyrimas:
3. Laboratorinis tyrimas:
Žmogaus kraujodaros kamieninių ląstelių
transplantacijos paslaugų, apmokamų iš
žmogaus organų ir audinių transplantacijos
paprastųjų išlaidų finansavimo programos
lėšų, teikimo reikalavimų, bazinių kainų ir
mokėjimo tvarkos aprašo
6 priedas
DONORO, kurį ketinama įtraukti į lietuvos negiminingų donorų registrą, ištyrimas
1. Klinikinis tyrimas:
Žmogaus kraujodaros kamieninių ląstelių
transplantacijos paslaugų, apmokamų iš
žmogaus organų ir audinių transplantacijos
paprastųjų išlaidų finansavimo programos
lėšų, teikimo reikalavimų, bazinių kainų ir
mokėjimo tvarkos aprašo
7 priedas
Negiminingo kraujodaros kamieninių ląstelių potencialaus donoro anketa
Prašome atidžiai užpildyti šią anketą. Jūsų atsakymai yra konfidencialūs. Tikslūs atsakymai į pateiktus klausimus svarbūs tam, kad būtų apsaugota Jūsų sveikata, bei tam, kad būtų apsaugotas pacientas, kuriam bus persodintos Jūsų kraujodaros kamieninės ląstelės. Pažymėkite tinkamus atsakymus – taip arba ne.
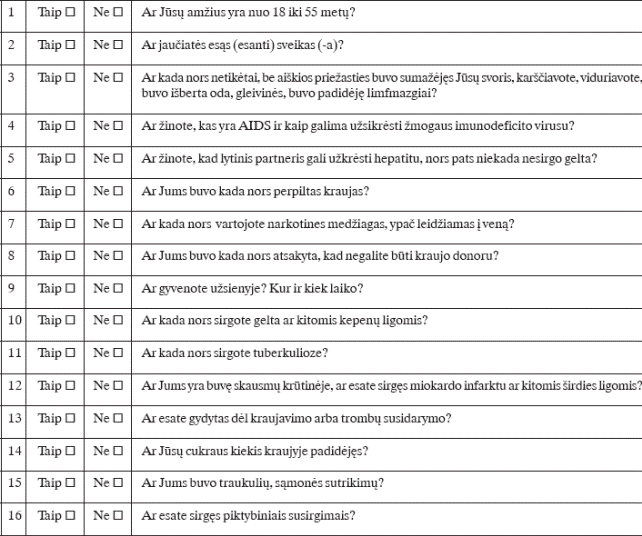
Prašome paaiškinti, jeigu į kuriuos nors klausimus, išskyrus 1, 2, 4 ir 5, atsakėte „taip“.
______________
Žmogaus kraujodaros kamieninių ląstelių
transplantacijos paslaugų, apmokamų iš
žmogaus organų ir audinių transplantacijos
paprastųjų išlaidų finansavimo programos
lėšų, teikimo reikalavimų, bazinių kainų ir
mokėjimo tvarkos aprašo
8 priedas
asmens sutikimas, kad jo duomenys būtų UŽregistruoti lietuvos negiminingų donorų registre
Sveikatos priežiūros įstaiga...................................................... ...................................................
(pavadinimas, kodas)
Aš,......................................................... .....................................................................................,
(vardas ir pavardė, asmens kodas)
................................................................................................................................................... ,
(telefonai, adresai)
sutinku, kad mano duomenys būtų įtraukti į Lietuvos negiminingų donorų registrą. Esu informuotas (-a) apie registro sudarymo tikslą, susipažinęs (-usi) su galima rizika, taip pat žinau, kad tapęs (-usi) savanoriu donoru negaliu tikėtis atlygio/užmokesčio.
Esu informuotas (-a), kad bet kada galiu atsisakyti šio sutikimo apie tai raštu pranešęs (-usi) Lietuvos negiminingų donorų registro tvarkytojui.
Pareiškiu, kad mano veiksnumas nėra ribotas.
Data........................................................................................................................................... .
Asmens parašas...........................................................................................................................
Informavusio gydytojo parašas, spaudas....................................................................................
______________
Pakeitimai:
1.
Lietuvos Respublikos sveikatos apsaugos ministerija, Įsakymas
Nr. V-300, 2005-04-27, Žin., 2005, Nr. 55-1886 (2005-04-30), i. k. 1052250ISAK000V-300
Dėl sveikatos apsaugos ministro 2004 m. rugsėjo 9 d. įsakymo Nr. V-632 "Dėl Žmogaus kraujodaros kamieninių ląstelių transplantacijos paslaugų, apmokamų iš Žmogaus organų ir audinių transplantacijos paprastųjų išlaidų finansavimo programos lėšų, teikimo reikalavimų, bazinių kainų ir mokėjimo tvarkos aprašo patvirtinimo" pakeitimo