
LIETUVOS RESPUBLIKOS SVEIKATOS APSAUGOS MINISTRAS
ĮSAKYMAS
DĖL ŽMOGAUS KRAUJODAROS KAMIENINIŲ LĄSTELIŲ TRANSPLANTACIJOS PASLAUGŲ, APMOKAMŲ IŠ TRANSPLANTACIJOS PROGRAMOS LĖŠŲ, TEIKIMO REIKALAVIMŲ, BAZINIŲ KAINŲ IR MOKĖJIMO TVARKOS APRAŠO PATVIRTINIMO
2019 m. rugpjūčio 2 d. Nr. V-965
Vilnius
Vadovaudamasis Lietuvos Respublikos sveikatos priežiūros įstaigų įstatymo 10 straipsnio 6 punktu:
1. T v i r t i n u Žmogaus kraujodaros kamieninių ląstelių transplantacijos paslaugų, apmokamų iš Transplantacijos programos lėšų, teikimo reikalavimus, bazines kainas ir mokėjimo tvarkos aprašą (pridedama).
2. P r i p a ž į s t u netekusiu galios Lietuvos Respublikos sveikatos apsaugos ministro 2004 m. rugsėjo 9 d. įsakymą Nr. V-632 „Dėl Žmogaus kraujodaros kamieninių ląstelių transplantacijos paslaugų, apmokamų iš Transplantacijos programos lėšų, teikimo reikalavimų, bazinių kainų ir mokėjimo tvarkos aprašo patvirtinimo“ su visais pakeitimais ir papildymais.
3. N u s t a t a u, kad:
3.1. šis įsakymas įsigalioja 2020 m. sausio 1 d.;
3.2. teisės aktuose nuoroda į Lietuvos Respublikos sveikatos apsaugos ministro 2004 m. rugsėjo 9 d. įsakymą Nr. V-632 „Dėl Žmogaus kraujodaros kamieninių ląstelių transplantacijos paslaugų, apmokamų iš Transplantacijos programos lėšų, teikimo reikalavimų, bazinių kainų ir mokėjimo tvarkos aprašo patvirtinimo“ laikoma nuoroda į šį įsakymą.
4. P a v e d u įsakymo vykdymo kontrolę viceministrui pagal veiklos sritį.
Laikinai einantis sveikatos apsaugos ministro pareigas Aurelijus Veryga
PATVIRTINTA
Lietuvos Respublikos sveikatos apsaugos
ministro 2004 m. rugsėjo 9 d. įsakymu Nr. V-632
(Lietuvos Respublikos sveikatos apsaugos
ministro 2019 m. rugpjūčio 2 d. įsakymo Nr. V-965
redakcija)
ŽMOGAUS KRAUJODAROS KAMIENINIŲ LĄSTELIŲ TRANSPLANTACIJOS PASLAUGŲ, APMOKAMŲ IŠ TRANSPLANTACIJOS PROGRAMOS LĖŠŲ, TEIKIMO REIKALAVIMŲ, BAZINIŲ KAINŲ IR MOKĖJIMO TVARKOS APRAŠAS
I SKYRIUS
BENDROSIOS NUOSTATOS
1. Autologinė kraujodaros kamieninių ląstelių transplantacija (AUTOKKLT) – kraujodaros kamieninių ląstelių paėmimas ir persodinimas į to paties žmogaus kūną gydymo tikslu.
2. Alogeninė kraujodaros kamieninių ląstelių transplantacija (ALOKKLT) – kraujodaros kamieninių ląstelių paėmimas ir persodinimas į kito žmogaus kūną gydymo tikslu. Skiriamos šios ALOKKLT rūšys:
2.1. gimininga ALOKKLT – donoras ir recipientas yra tų pačių tėvų vaikai;
2.2. negimininga ALOKKLT – donoras ir recipientas yra skirtingų tėvų vaikai;
2.3. haploidentinė ALOKKLT – donoras ir recipientas yra tų pačių ar skirtingų tėvų vaikai ir skiriasi daugiau kaip vienu I ir (ar) II klasės žmogaus leukocitų antigenu.
3. Kraujodaros kamieninių ląstelių šaltiniai:
3.2. periferinis kraujas;
3.3. placenta ir placentinis kraujas po vaiko gimimo.
4. Lietuvos negiminingų donorų registras (LNDR) yra Žmogaus audinių, ląstelių ir organų donorų bei recipientų registro sudėtinė dalis.
5. Sprendimas, ar atlikti kraujodaros kamieninių ląstelių transplantaciją, priimamas laikantis šių nuostatų:
5.1. Sprendimas, ar atlikti kraujodaros kamieninių ląstelių transplantaciją, priimamas individualiai, atsižvelgiant į ligą, jos stadiją, prognozę, donoro buvimą bei tikimybę donorą rasti tinkamu laiku, bendrą paciento būklę, organų funkciją bei kitus medicininius ir socialinius veiksnius.
5.2. Kraujodaros kamieninių ląstelių transplantacija gali būti atliekama tik pacientams, kurių būklė pagal Pasaulio sveikatos organizacijos bendrosios būklės rodiklį vertinama ne daugiau kaip (PSO) 2 (1 priedas).
5.3. Sprendimą, ar atlikti kraujodaros kamieninių ląstelių transplantaciją, priima gydytojų konsiliumas (toliau – Konsiliumas). Konsiliume dalyvaujantys gydytojai specialistai sprendimus gali priimti tik neviršydami jų medicinos normose ir kituose teisės aktuose nustatytų kompetencijų. Sprendimas įrašomas Konsiliumo dėl indikacijų kraujodaros kamieninių ląstelių transplantacijai atlikti protokole (2 priedas). Šis protokolas saugomas kartu su pildomais medicinos dokumentais (ligonio gydymo stacionare ligos istorija Nr. 003/a ar asmens sveikatos istorija Nr. 025/a). Už Konsiliumų organizavimą atsakingas kraujodaros kamieninių ląstelių transplantacijas atliekančio padalinio vadovas.
6. Pacientų, kuriems bus atliekama kraujodaros kamieninių ląstelių transplantacija (toliau – KKLT), sąrašo sudarymo principai:
6.1. Į pacientų, kuriems bus atliekama kraujodaros kamieninių ląstelių transplantacija, sąrašą įtraukiami pacientai, dėl kurių Konsiliumas pateikia išvadą dėl indikacijų atlikti KKLT (Konsiliumo dėl indikacijų kraujodaros kamieninių ląstelių transplantacijai atlikti protokolas (2 priedas)) ir kurie raštu sutinka, kad jiems būtų atlikta transplantacija (3 priedas). Vaikų iki 18 metų raštišką sutikimą pasirašo Lietuvos Respublikos pacientų teisių ir žalos sveikatai atlyginimo įstatyme nurodyti atstovai (toliau – paciento atstovas).
6.2. Iš pacientų, kuriems bus atliekama kraujodaros kamieninių ląstelių transplantacija, sąrašo išregistruojami šie pacientai:
6.2.1. atsisakę transplantacijos;
6.2.2. mirę iki transplantacijos;
6.2.3. kuriems nustatytos nuolatinės kontraindikacijos transplantacijai atlikti, patvirtintos pakartotinio Konsiliumo;
6.2.4. kuriems išnyko indikacijos transplantacijai atlikti, patvirtintos pakartotinio Konsiliumo;
6.2.5. apie kuriuos nepavyksta gauti duomenų ilgiau kaip 6 mėn.;
6.2.6. kuriems pradėtas vienas iš transplantacijos etapų.
6.3. Sprendimas išregistruoti pacientą iš sąrašo įrašomas Konsiliumo dėl indikacijų kraujodaros kamieninių ląstelių transplantacijai atlikti protokole (2 priedas). Šis protokolas saugomas kartu su pildomais medicinos dokumentais (ligonio gydymo stacionare ligos istorija Nr. 003/a ar asmens sveikatos istorija Nr. 025/a).
6.4. Už sąrašo sudarymą ir saugojimą atsako transplantacijos padalinio vadovas.
6.5. Sąrašas peržiūrimas ne rečiau kaip kas 3 mėn.
7. Skubos tvarka atliekama kraujodaros kamieninių ląstelių transplantacija, jei tenkinamos visos šios sąlygos:
7.1. pacientui KKLT gali būti atliekama skubos tvarka, jei jam nustatytos skubios transplantacijos medicininės indikacijos;
7.2. transplantacija turi būti atliekama kuo skubiau, kai tik mediciniškai ir techniškai įmanoma;
7.3. sprendimas transplantaciją atlikti skubos tvarka turi būti patvirtintas Konsiliumo. Konsiliumo išvados įrašomos į Konsiliumo dėl indikacijų kraujodaros kamieninių ląstelių transplantacijai atlikti protokolą (2 priedas). Šis protokolas saugomas kartu su pildomais medicinos dokumentais (ligonio gydymo stacionare ligos istorija Nr. 003/a ar asmens sveikatos istorija Nr. 025/a). Už Konsiliumų organizavimą atsakingas kraujodaros kamieninių ląstelių transplantacijos padalinio vadovas;
7.4. pacientai, kuriems transplantaciją būtina atlikti skubos tvarka, įrašomi į pacientų, kuriems bus atliekama kraujodaros kamieninių ląstelių transplantacija, sąrašą ir greta jų pavardžių pažymima „skubi transplantacija“.
II SKYRIUS
ŽMOGAUS KRAUJODAROS KAMIENINIŲ LĄSTELIŲ TRANSPLANTACIJOS PASLAUGŲ TEIKIMO REIKALAVIMAI
8. Asmens sveikatos priežiūros įstaiga (toliau – įstaiga), kurioje atliekama kraujodaros kamieninių ląstelių transplantacija, yra universiteto ligoninė, turinti tretinės stacionarinės suaugusiųjų hematologijos (kai teikiamos suaugusiųjų transplantacijos paslaugos) ir (ar) tretinės vaikų onkohematologijos (kai teikiamos vaikų transplantacijos paslaugos), kraujo donorystės (kraujo centro), audinių banko (kraujo kamieninių ląstelių paėmimas, apdorojimas, paskirstymas ir laikymas) asmens sveikatos priežiūros licencijas. Įstaigoje KKLT atlieka suaugusiųjų KKLT padalinys ir (ar) vaikų KKLT padalinys ar jungtinis suaugusiųjų ir vaikų KKLT padalinys (atliekant KKLT jungtiniame suaugusiųjų ir vaikų KKLT padalinyje, paslaugos teikiamos pagal medicinos normose ir kituose teisės aktuose nustatytą gydytojo kompetenciją).
9. Įstaigoje turi būti įrengtos mažiausiai 2 iš dalies izoliuotos vienvietės intensyviosios terapijos palatos, kuriose turi būti:
9.1. įrengtas atskiras sanitarinis mazgas;
9.2. rankų dezinfekcijos priemonės;
9.3. laminarinė teigiamo spaudimo didelio efektyvumo dalelių (HEPA) ar lygiavertė filtruoto oro tėkmė;
9.4. paciento gyvybinių funkcijų stebėsenos įrenginys;
9.5. deguonies tiekimo sistema.
10. Įstaiga, kurioje atliekamos kraujodaros kamieninių ląstelių transplantacijos, privalo atitikti šiuos specialiuosius reikalavimus:
10.1. Įstaigoje turi būti audinių banko veiklą vykdantis padalinys, turintis programuojamo šaldymo bei skysto azoto ilgo laikymo įrangą.
10.2. Įstaigoje turi būti aferezių padalinys, turintis ne mažiau kaip 2 ląstelių aferezės aparatus, kurie gali atlikti:
10.2.1 eritrocitaferezę, trombocitaferezę, leukaferezę, viso cirkuliuojančio plazmos tūrio pakeitimą (plazmaferezę), kraujodaros kamieninių ląstelių aferezę, limfocitaferezę;
10.2.2. kai atliekama ALOKKLT – fotoferezę, surinktų kaulų čiulpų tūrio sumažinimą.
10.3. Įstaigoje turi būti užtikrintas nepertraukiamas šių kraujo komponentų tiekimas transplantuojamiems pacientams ištisą parą:
10.3.1. apšvitintų jonizuojančiaisiais spinduliais leukocitų (inaktyvacijos tikslu);
10.3.2. kai atliekamos ALOKKLT:
10.3.2.1. citomegalo virusui neigiamų kraujo komponentų;
10.3.2.2. trombocitų, suderintų pagal žmogaus leukocitų antigenus (ŽLA), žmogaus trombocitų antigenus (ŽTA), taip pat kryžmiškai suderintų aferezinių trombocitų be leukocitų;
10.3.2.3. trombocitų, šviežiai šaldytos plazmos, kuriems taikyta patogenų redukcija;
10.3.2.4. eritrocitų, trombocitų, šviežiai šaldytos plazmos bei krioprecipitato be leukocitų.
10.4. KKLT registruojamos ir informacija apie transplantacijų rezultatus kaupiama įstaigos transplantacijų registracijos ir jų rezultatų stebėsenos sistemoje. Sistemoje turi būti kaupiama ši informacija (atnaujinama ne rečiau kaip kas 3 mėnesius): donoro vardas, pavardė, asmens kodas, kraujodaros kamieninių ląstelių šaltinis (kraujas, kaulų čiulpai, kt.), donacijos data; recipiento vardas, pavardė, asmens kodas, transplantacijos indikacija, ligos, dėl kurios atliekama transplantacija, kodas pagal TLK-10-AM, remisijos būklė prieš pat transplantaciją, gretutinės ligos transplantacijos metu, transplantacijos data, kondicionavimo režimas, transplantato prigijimo data, ligos atsinaujinimo data, mirties data bei jos priežastis. Duomenys apie KKLT teikiami Nacionaliniam transplantacijos biurui prie Sveikatos apsaugos ministerijos. Informacija apie per praėjusius kalendorinius metus įstaigoje atliktų transplantacijų skaičių, jų rūšį (autologinė, alogeninė) viešai skelbiama įstaigos interneto tinklalapyje ne vėliau kaip iki einamųjų metų kovo 31 d.
11. Įstaigoje turi būti atliekami šie specialieji tyrimai (pačioje įstaigoje ar kitose įstaigose, su kuriomis sudaryta sutartis):
11.1. tėkmės citometrijos tyrimai kraujodaros kamieninių ląstelių koncentracijai kraujyje ir aferezės produktuose bei jų gyvybingumui nustatyti;
11.2. imunosupresorių ir citostatikų koncentracijos kraujyje tyrimai;
11.3. pacientams, esantiems imunosupresinės būklės, svarbūs infekciniai tyrimai: infekciniai molekuliniai kokybiniai (bakterijų, atipinių bakterijų, virusų, pirmuonių, grybų, kt. sukėlėjų) tyrimai; infekciniai molekuliniai kiekybiniai citomegalo viruso ir Epstein-Barro, hepatitų B ir C virusų tyrimai; Pneumocystis jiroveci, Clostridium difficile toksino, aspergiliozės tyrimai.
11.4. Žmogaus kariotipo citogenetinis, onkohematologiniai molekulinės biologijos tyrimai.
12. Autologinės žmogaus kraujodaros kamieninių ląstelių transplantacijos paslaugų teikimo reikalavimai:
12.1. Specialieji reikalavimai įstaigai, kuri teikia autologinės kraujodaros kamieninių ląstelių transplantacijos paslaugas:
12.1.1. įstaigoje AUTOKKLT gali būti atliekama tik po to, kai ne trumpiau kaip 5 metus buvo sistemingai taikoma didelių dozių chemoterapija onkohematologinėms ir (arba) onkologinėms ligoms gydyti;
12.1.2. AUTOKKLT paslaugas teikiančiam padaliniui (suaugusiųjų, vaikų arba jungtiniam) vadovauja ne trumpesnį kaip 2 metų KKLT atlikimo patirtį turintis gydytojas hematologas ar vaikų onkohematologas;
12.1.3. AUTOKKLT paslaugas teikiančiame padalinyje turi dirbti bent 1 gydytojas hematologas (kai atliekamos AUTOKKLT suaugusiesiems) ar bent 1 vaikų onkohematologas (kai atliekamos AUTOKKLT vaikams), turintys ne trumpesnę kaip 1 metų darbo patirtį atliekant KKLT arba ne trumpiau kaip 1 metus stažavęsi KKLT procedūras atliekančiame centre. Gydytojų skaičius padalinyje turi būti pakankamas, kad šių gydytojų teikiamų AUTOKKLT paslaugų teikimas būtų užtikrintas nepertraukiamu paros (įskaitant poilsio ir švenčių dienas) darbo režimu;
12.1.4. AUTOKKLT paslaugas teikiančiame padalinyje turi dirbti bendrosios praktikos slaugytojai, turintys ne trumpesnę kaip 1 metų KKLT pacientų slaugymo patirtį arba ne trumpiau kaip 1 metus stažavęsi KKLT procedūras atliekančiame centre. Padalinyje turi būti pakankamai slaugytojų, kad jų teikiamų AUTOKKLT paslaugų teikimas būtų užtikrintas nepertraukiamu paros (įskaitant poilsio ir švenčių dienas) darbo režimu;
12.1.5. per metus (skaičiuojamas dvejų metų iš eilės vidurkis) įstaigoje turi būti atliekamos ne mažiau kaip 5 AUTOKKLT suaugusiesiems (kai teikiamos suaugusiųjų AUTOKKLT paslaugos) ir 5 AUTOKKLT vaikams (kai teikiamos vaikų AUTOKKLT paslaugos). Jungtiniame AUTOKKLT padalinyje per metus turi būti atliekamos ne mažiau kaip 5 vaikų ir 5 suaugusiųjų AUTOKKLT.
12.2. Indikacijos atlikti autologinę kraujodaros kamieninių ląstelių transplantaciją:
| Diagnozė |
TLK-10-AM kodai |
Papildomos sąlygos |
| Ūmi mieloleukemija |
C92.0, C92.2–C92.7, C93.0, C93.2, C93.7, C93.9, C94.0, C94.2–C94.5 |
Visiška remisijaa |
| Ūmi limfoleukemija |
C91.0, C91.2–C91.7, C91.9 |
Visiška remisijaa |
| Ūmi bifenotipė leukemija, ūmi patikslinta leukemija |
C94.7, C95.0 |
Visiška remisijaa |
| Mielodisplazijos sindromas su blastų pertekliumi |
D46.2 |
Visiška remisijaa |
| Lėtinė mieloleukemija |
C92.1 |
Lėtinė fazėb |
| Lėtinė limfoleukemija |
C91.1 |
Progresavimasc Remisija |
| Ne Hodžkino limfoma, piktybinės imunoproliferacinės ligos |
C82–C85, C88 |
Progresavimasd Atkrytise Pirminė liga, kai tarptautinis prognozės indeksas (IPI) > 1 (agresyvios, ne Hodžkino limfomos) |
| Hodžkino limfoma |
C81 |
Progresavimasd Atkrytis po chemoterapijose |
| Mielominė liga |
C90 |
Indikuotina |
| Histiocitozė ir hemofagocitiniai sindromai |
C96, D76 |
Piktybinė forma Progresavimasd Atkrytise |
| Germinogeniniai navikai |
C37, C56, C62, C71, C72, C73 |
Didelės rizikos pirminiai navikaif Progresavimasd Atkrytise |
| Ewingo sarkoma, PNET |
C00–C06, C30, C31, C38, C40, C41, C47–C49, C69, C74 |
Didelės rizikos pirminiai navikaig Progresavimasd Atkrytise |
| Neuroblastoma |
C00–C06, C30, C31, C38, C40, C41, C47–C49, C69, C74 |
Didelės rizikos pirminiai navikaih Atkrytise |
| Vaikų amžiui būdingi smegenų piktybiniai navikai |
C71, C72 |
Didelės rizikos pirminiai navikai Progresavimasd Atkrytis |
| Rabdoidiniai navikai |
C00-C06, C30, C31, C40–41, C47–C49, C64–C68, C69, C71 |
Didelės rizikos pirminiai navikai Progresavimasd Atkrytise |
| Išsėtinė sklerozėi |
G35 |
1. Recidyvuojanti remituojanti išsėtinė sklerozė. 2. Neefektyvus šiuolaikinis ligos eigą imunomoduliuojantis gydymas. 3. Negalia pagal išplėstinę negalios vertinimo skalę (EDSS) 4,0–6,0 balai ir neįgalumo progresavimas (neįgalumo padidėjimas dviem ir daugiau balų pagal EDSS skalę per vienus metus). 4. Agresyvi eiga pastarųjų dvejų metų laikotarpiu (bent du kriterijai): 4.1. ≥1 sunkus ligos paūmėjimas – EDSS padidėjimas daugiau kaip 1 balu, apimantis motorinius, smegenėlinius ir (arba) kamieninius simptomus ir (arba) dalinis negalios regresavimas po sunkaus paūmėjimo; 4.2. per praėjusius metus buvo bent du gliukokortikoidais gydyti recidyvai arba bent 1 gliukokortikoidais gydytas recidyvas ir papildomai vienas gadolinį (Gd) kaupiantis MBR židinys kitu metu; 4.3. galvos smegenų MRT nustatyti ne mažiau kaip devyni T2 režime hiperintensiniai židiniai, vienas gadolinį kaupiantis židinys ir naujai atsiradęs ≥3mm dydžio ≥1 Gd+ židiniai (-ys) arba ≥0,3 T2 židinių daugėjimas per mėnesį, vertinamas dviejuose iš eilės atliktuose galvos smegenų MRT tyrimuose, tarp kurių atlikimo praėjo 6–12 mėnesių. |
| Sisteminė sklerozėj |
M34.0 |
Progresuojanti sisteminė sklerozė (odos pažeidimas proksimaliau alkūnių ir kelių, modifikuota Rodnano odos pažeidimo skalė >14), kai pastebimas refrakterumas standartiniam gydymui ir nustatytas bent vienas iš šių kriterijų: 1. plaučiai: dujų difuzija mažiau nei 80 proc. normos ir (arba) sumažėjusi gyvybinė plaučių talpa 10 proc. ar daugiau per paskutinius 12 mėnesių ir (ar) yra plaučių fibrozė arba matinio stiklo zonų (nustatoma atliekant plaučių KT); 2. širdis: laidumo pakitimai EKG ir (arba) perikardo pažeidimo požymiai (nustatomi MRT tyrimu); 3. virškinamojo trakto pažeidimas (patvirtintas radiologiškai). |
PASTABOS:
a – Mažiau kaip 5 proc. leukemijos blastų kaulų čiulpuose.
b – Mažiau kaip 10 proc. leukemijos blastų periferiniame kraujyje ar kaulų čiulpuose, mažiau kaip 20 proc. leukemijos blastų ir promielocitų kraujyje ar kaulų čiulpuose.
c – Bent vienas iš požymių: limfocitozės, limfmazgių, organų didėjimas, progresuojanti anemija, neutropenija, trombocitopenija.
d – Bent vienas iš požymių: išliekantys sisteminiai ligos simptomai, naujų ligos požymių atsiradimas, mažesnė kaip 50 proc. regresija, teigiamas pozitroninės emisinės tomografijos tyrimo rezultatas.
e – Ligos atsinaujinimas po visiškos ar dalinės remisijos.
f – Ne seminoma ir bent vienas iš požymių: pirminis tarpuplaučio navikas, ne plaučių metastazės, AFP > 10 000 ng/ml, hCG > 50 000 IU/ml, LDH > 10 kartų didesnė už viršutinę normos ribą.
g – Bent vienas iš požymių: metastazės, naviko nekrozė po indukcinės chemoterapijos < 90 proc., pirminio naviko tūris > 200 ml ir neįvertinama naviko nekrozė po chemoterapijos, aksialinis navikas.
h – Bent vienas iš požymių: IV stadija, I–III stadija ir MYCN amplifikacija, blogas atsakas į standartinę chemoterapiją.
i – Sprendimą dėl AUTOKKLT tikslingumo priima universiteto ligoninės gydytojų konsiliumas (ne mažiau kaip trys gydytojai neurologai (vaikų neurologai), gydytojas hematologas (vaikų onkohematologas) ir gydytojas radiologas), kai išsėtinės sklerozės diagnozė patvirtinta vadovaujantis 2010 m. McDonaldo kriterijais.
j – Sprendimą dėl AUTOKKLT tikslingumo priima universiteto ligoninės gydytojų konsiliumas (ne mažiau kaip trys gydytojai reumatologai (vaikų reumatologai), gydytojas hematologas (vaikų onkohematologas) ir gydytojas radiologas).
12.3. Autologinę kraujodaros kamieninių ląstelių transplantaciją sudaro:
12.3.1. potencialaus recipiento sutikimas, kad jam būtų atlikta autologinė kraujodaros kamieninių ląstelių transplantacija (3 priedas);
12.3.2. potencialaus recipiento ištyrimas (5 priedas);
12.3.3. kraujodaros kamieninių ląstelių mobilizacija granulocitų kolonijas stimuliuojančiu veiksniu ir (ar) citostatikais, surinkimas, užšaldymas ir laikymas;
12.3.4. recipiento kondicionavimas, kraujodaros kamieninių ląstelių infuzija į recipiento veną, pradinis laikotarpis po AUTOKKLT, kai būtina hospitalizuoti recipientą;
12.3.5. laikotarpis po AUTOKKLT, kai būtina aktyviai ambulatoriškai stebėti ir gydyti recipientą;
12.3.6. vėlyvųjų komplikacijų po AUTOKKLT, dėl kurių būtina recipientą hospitalizuoti, tyrimas ir gydymas;
12.3.7. transplantuotų pacientų stebėsena užtikrinama KKLT atlikusioje įstaigoje.
13. Alogeninės kraujodaros kamieninių ląstelių transplantacijos paslaugų teikimo reikalavimai:
13.1. Specialieji reikalavimai Įstaigai, kuri teikia alogeninės kraujodaros kamieninių ląstelių transplantacijos paslaugas:
13.1.1 Įstaigoje ALOKKLT gali būti atliekama tik po to, kai ne trumpiau kaip 5 metus buvo sistemingai taikoma didelių dozių chemoterapija onkohematologinėms ir (arba) onkologinėms ligoms gydyti ir ne trumpiau kaip 2 metus atliekamos AUTOKKLT;
13.1.2. ALOKKLT paslaugas teikiančiam padaliniui (suaugusiųjų, vaikų arba jungtiniam) vadovauja ne trumpesnį kaip 2 metų ALOKKLT atlikimo patirtį turintis gydytojas hematologas ar vaikų onkohematologas;
13.1.3. ALOKKLT paslaugas teikiančiame padalinyje turi dirbti bent 1 gydytojas hematologas (kai atliekamos ALOKKLT suaugusiesiems) ar bent 1 vaikų onkohematologas (kai atliekamos ALOKKLT vaikams), turintys ne trumpesnę kaip 1 metų darbo patirtį atliekant ALOKKLT arba ne trumpiau kaip 1 metus stažavęsi ALOKKLT procedūras atliekančiame centre. Gydytojų skaičius padalinyje turi būti pakankamas, kad šių gydytojų teikiamų ALOKKLT paslaugų teikimas būtų užtikrintas nepertraukiamu paros (įskaitant poilsio ir švenčių dienas) darbo režimu;
13.1.4. ALOKKLT paslaugas teikiančiame padalinyje turi dirbti bendrosios praktikos slaugytojai, turintys ne trumpesnę kaip 1 metų KKLT pacientų slaugymo patirtį arba ne trumpiau kaip 1 metus stažavęsi KKLT procedūras atliekančiame centre. Padalinyje turi būti pakankamai slaugytojų, kad jų teikiamų ALOKKLT paslaugų teikimas būtų užtikrintas nepertraukiamu paros (įskaitant poilsio ir švenčių dienas) darbo režimu;
13.1.5. per metus (skaičiuojamas dvejų metų iš eilės vidurkis) įstaigoje turi būti atliekamos ne mažiau kaip 10 ALOKKLT suaugusiesiems (kai teikiamos suaugusiųjų ALOKKLT paslaugos) ir 5 ALOKKLT vaikams (kai teikiamos vaikų ALOKKLT paslaugos). Jungtiniame ALOKKLT padalinyje per metus turi būti atliekama 5 vaikų ir 5 suaugusiųjų ALOKKLT;
13.1.6. Įstaigoje turi būti atliekami šie specialieji tyrimai (pačioje įstaigoje ar kitose įstaigose, su kuriomis sudaryta sutartis) bei procedūros:
13.1.6.1. didelės skiriamosios gebos I ir II klasės žmogaus leukocitų antigenų ŽLA tyrimai;
13.1.6.2. donoro-recipiento leukocitų bendrojo bei leukocitų populiacijų chimerizmo tyrimai;
13.1.6.3. minimalios likutinės ligos stebėsenos kraujyje bei kaulų čiulpuose molekulinės genetikos, imunotipavimo metodais tyrimai;
13.1.6.4. citotoksinių limfocitų, mezenchiminių ląstelių, kraujodaros kamieninių ląstelių selekcijos procedūros.
13.2. Indikacijos atlikti alogeninę kraujodaros kamieninių ląstelių transplantaciją:
| Diagnozė |
TLK-10-AM kodai |
Papildomos sąlygos |
| |
|
Gimininga |
Negimininga |
| Ūmi mieloleukemija |
C92.0, C92.2–C92.7, C93.0, C93.2, C93.7, C93.9, C94.0, C94.2-C94.5 |
Visiškaa ar dalinėb remisija ar prasidedantis atkrytisc |
Visiškaa ar dalinėb remisija ar prasidedantis atkrytisc |
| Ūmi limfoleukemija |
C91.0, C91.2–C91.7, C91.9 |
Visiškaa ar dalinėb remisija ar prasidedantis atkrytisc |
Visiškaa ar dalinėb remisija ar prasidedantis atkrytisc |
| Ūmi bifenotipė leukemija, ūmi patikslinta leukemija |
C95.0, C94.7 |
Visiškaa ar dalinėb remisija ar prasidedantis atkrytisc |
Visiškaa ar dalinėb remisija ar prasidedantis atkrytisc |
| Mielodisplazijos sindromas |
D46, C93.1 |
Indikuotina |
Indikuotina |
| Lėtinė mieloleukemija |
C92.1 |
Lėtinėd ar akceleracijose stadija |
Lėtinėd ar akceleracijose stadija |
| Lėtinė mieloproliferacinė liga |
D47.1 |
Progresavimasf |
Progresavimasf |
| Lėtinė limfoleukemija |
C91.1 |
Progresavimasg ar remisija |
Progresavimasg ar remisija |
| Ne Hodžkino limfoma, piktybinės imunoproliferacinės ligos |
C82–C85, C88 |
Progresavimash ar atkrytisi |
Progresavimash ar atkrytisi |
| Hodžkino limfoma |
C81 |
Progresavimash ar atkrytisi |
Progresavimash ar atkrytisi |
| Mielominė liga |
C90 |
Indikuotina |
Indikuotina |
| Aplazinė anemija, eritropoezės aplazija |
D60, D61 |
Indikuotina |
Indikuotina |
| Talasemija |
D56 |
Sunkios formos |
Sunkios formos |
| Histiocitozė ir hemofagocitiniai sindromai |
C96, D76 |
piktybinė forma ar ar progresavimash Atkrytisi |
Piktybinė forma ar progresavimash,ar atkrytisi |
| Germinogeniniai navikai |
C37, C56, C62, C71, C72, C73 |
Kai indikuotina AUTOKKLT, tačiau dėl techninių kliūčių jos atlikti neįmanoma |
Neindikuotina |
| Ewingo sarkoma, PNET |
C00–C06, C30, C31, C38, C40, C41, C47-C49, C69, C74 |
Kai indikuotina AUTOKKLT, tačiau dėl techninių kliūčių jos atlikti neįmanoma |
Neindikuotina |
| Įgimti kraujodaros, medžiagų apykaitos sutrikimai, imunodeficitai (įgimta diseritropoezinė anemija, įgimta amegakariocitinė trombocitopenija, trombocitopenija su nesančiu stipinkauliu, agranulocitozė, kombinuotas imunodeficitas, kiti imunodeficitai, Wiskotto-Aldricho sindromas, medžiagų apykaitos sutrikimai su kraujodaros sistemos pažeidimu, adrenoleukodistrofija) |
D64, D69.4, D70, D71, D81, D82, E71, E75–E77, Q87 |
Sunkios formos |
Sunkios formos |
PASTABOS:
a – Mažiau kaip 5 proc. leukemijos blastų kaulų čiulpuose.
b – 6–20 proc. leukemijos blastų kaulų čiulpuose.
c – Pogresuojanti neutropenija, anemija, trombocitopenija ir mažiau kaip 5 proc. leukemijos blastų kaulų čiulpuose.
d – Mažiau kaip 10 proc. leukemijos blastų periferiniame kraujyje ar kaulų čiulpuose, mažiau kaip 20 proc. leukemijos blastų ir promielocitų kraujyje ar kaulų čiulpuose.
e – Leukemijos blastų kaulų čiulpuose yra 10–19 proc., leukemijos blastų ir promielocitų kraujyje ar kaulų čiulpuose – 20–29 proc.
f – Bent vienas iš požymių: leukocitozės, organų didėjimas, progresuojanti anemija, neutropenija, trombocitopenija.
g – Bent vienas iš požymių: limfocitozės, limfmazgių, organų didėjimas, progresuojanti anemija, neutropenija, trombocitopenija.
h – Bent vienas iš požymių: išliekantys sisteminiai ligos simptomai, naujų ligos požymių atsiradimas, mažesnė kaip 50 proc. regresija, teigiamas pozitroninės emisinės tomografijos tyrimo rezultatas.
i – Ligos atsinaujinimas po visiškos ar dalinės remisijos.
13.3. Alogeninę kraujodaros kamieninių ląstelių transplantaciją sudaro:
13.3.1. potencialaus donoro sutikimas, kad jo kraujodaros kamieninės ląstelės būtų panaudotos transplantacijai (4 priedas);
13.3.2. potencialaus recipiento sutikimas, kad jam būtų atlikta ALOKKLT (3 priedas);
13.3.3. potencialaus donoro ir recipiento ištyrimas (5 priedas);
13.3.4. potencialaus donoro ir recipiento ŽLA tipavimas;
13.3.5. gimininga ar haploidentiška ALOKKLT: giminingo ar haploidentiško donoro kraujodaros kamieninių ląstelių mobilizacija granulocitų kolonijas stimuliuojančiu veiksniu bei kamieninių ląstelių surinkimas ląstelių aferezės aparatu arba iš kaulų čiulpų;
13.3.6. negimininga ALOKKLT: donoro paieška, jo kvietimas ir ištyrimas, kraujodaros kamieninių ląstelių surinkimas bei atvežimas. Negiminingų donorų ALOKKLT paslaugas teikianti įstaiga skiria koordinatorių, kuris tvarko dokumentus, atlieka negiminingo KKL donoro paiešką per koordinuojančią įstaigą, organizuoja KKL gabenimą;
13.3.7. recipiento kondicionavimas, donoro kraujodaros kamieninių ląstelių infuzija į recipiento veną, pradinis laikotarpis po ALOKKLT, kai reikia hospitalizuoti recipientą;
13.3.8. laikotarpis po ALOKKLT, kai reikia aktyviai ambulatoriškai stebėti ir gydyti recipientą;
13.3.9. vėlyvųjų komplikacijų po ALOKKLT, dėl kurių būtina recipientą hospitalizuoti, tyrimas ir gydymas;
13.3.10. transplantuotų pacientų stebėsena užtikrinama KKLT atlikusioje įstaigoje.
III SKYRIUS
ALOGENINIŲ NEGIMININGŲ DONORŲ KAULŲ ČIULPŲ TRANSPLANTACIJŲ KOORDINAVIMAS IR NEGIMININGŲ DONORŲ PAIEŠKA
14. Negiminingų donorų ALOKKLT koordinavimo paslaugas teikianti įstaiga:
14.1. bendradarbiauja su ALOKKLT paslaugas teikiančios įstaigos paskirtu koordinatoriumi nustatant negiminingo donoro paieškos strategiją, atsižvelgdama į ŽLA tapatumą, rasę, amžių, lytį, kraujo grupę, infekuotumą citomegalijos virusu, negiminingo donoro paieškos, jo kvietimo ir ištyrimo, bei kamieninių ląstelių surinkimo išlaidas;
14.2. atlieka negiminingo KKL donoro paiešką;
14.3. esant poreikiui atlieka negiminingo donoro ištyrimą prieš kraujodaros kamieninių ląstelių donaciją pagal šio tvarkos aprašo 5 priedą ir atlieka ląstelių surinkimą;
14.4. telkia potencialius negiminingus kraujodaros kamieninių ląstelių donorus ir teikia duomenis Lietuvos negiminingų donorų registrui (LNDR);
14.5. prireikus suteikia rekomendaciją siųsti pacientą negiminingo donoro ALOKKLT atlikti į užsienio valstybes;
14.6. sprendžia kitus su negiminingų donorų ALOKKLT atlikimu susijusius klausimus.
15. Specialieji reikalavimai negiminingų donorų ALOKKLT koordinavimo paslaugas teikiančiai įstaigai:
15.1. įstaigoje turi būti hematologijos padalinys, kuris ne trumpiau kaip 5 metus atlieka ALOKKLT ir per šį periodą yra atlikęs ne mažiau kaip 40 ALOKKLT;
15.2. turi turėti prieigą prie Lietuvos negiminingų donorų registro (LNDR);
15.3. įstaigoje turi būti atliekami imunogenetikos tyrimai:
15.3.1. didelės skiriamosios gebos I ir II klasės antigenų ŽLA nustatymas;
15.3.2. turi dalyvauti Europos imunogenetikos federacijos (EFI) ar lygiavertėje tarptautinėje imunogenetinių tyrimų akreditacijos programoje.
16. Negiminingų donorų atranka į Lietuvos negiminingų donorų registrą (LNDR):
16.1. negiminingais kraujodaros kamieninių ląstelių donorais gali būti ne jaunesni kaip 18 metų ir ne vyresni kaip 55 metų asmenys savanoriai;
16.2. kontraindikacijos įtraukti į negiminingų donorų registrą:
16.2.1. potencialaus donoro priklausymas didelės infekcijų perdavimo rizikos grupei;
16.2.2. lėtinė plaučių, širdies, inkstų, kepenų liga su funkcijos nepakankamumu;
16.2.3. onkologinės ligos, išskyrus plokščialąstelinį odos vėžį ar bazaliomą;
16.2.4. kraujo ligos, išskyrus alimentarinę anemiją;
16.2.5. sisteminės jungiamojo audinio ligos;
16.2.6. degeneracinės nervų sistemos ligos;
16.2.7. tromboembolija anamnezėje;
16.2.8. žmogaus imunodeficito viruso antikūnų, hepatito B paviršinio antigeno, sifilio arba hepatito C viruso antikūnų teigiami laboratorinių tyrimų rezultatai.
17. Potencialaus negiminingo donoro įrašymo į Lietuvos negiminingų donorų registrą (LNDR) tvarka:
17.1. Asmuo, norintis tapti negiminingu kraujodaros kamieninių ląstelių donoru, kreipiasi į įstaigą, kuri organizuoja jo ištyrimą (6 priedas).
17.2. Asmuo, kuris nori būti įregistruotas kaip negiminingas kraujodaros kamieninių ląstelių potencialus donoras, užpildo Negiminingo kraujodaros kamieninių ląstelių potencialaus donoro anketą (7 priedas) bei Asmens sutikimo, kad jo duomenys būtų užregistruoti Lietuvos negiminingų donorų registre formą (8 priedas). Pasirašydamas donoro anketą, asmuo patvirtina, kad jam buvo pateikti šios anketos klausimai, ir atsako už informacijos teisingumą.
17.3. Jei nėra klinikinių bei laboratorinių kontraindikacijų potencialų donorą registruoti Lietuvos negiminingų donorų registre (LNDR), įstaiga potencialaus donoro kraujo mėginius, anketos, sutikimo originalus bei šio tvarkos aprašo 17.1 papunktyje numatytus tyrimų rezultatus siunčia į negiminingų ALOKKLT koordinavimo paslaugas teikiančią įstaigą.
17.4. Negiminingų ALOKKLT koordinavimo paslaugas teikianti įstaiga organizuoja šių tyrimų atlikimą:
17.4.1. ŽLA I klasės antigenų (ŽLA – A, B, C) nustatymo tyrimą limfocitotoksiniu ar molekulinės biologijos metodu;
17.4.2. ŽLA II klasės antigenų (ŽLA – DR) nustatymo tyrimą molekulinės biologijos metodu.
17.5. Negiminingų ALOKKLT koordinavimo paslaugas teikianti įstaiga potencialaus donoro asmens ir laboratorinių tyrimų rezultatų duomenis siunčia į Lietuvos negiminingų donorų registrą (LNDR).
IV SKYRIUS
MOKĖJIMO UŽ ŽMOGAUS KRAUJODAROS KAMIENINIŲ LĄSTELIŲ TRANSPLANTACIJOS PASLAUGAS TVARKA
18. Teritorinė ligonių kasa (toliau – TLK) pagal šio tvarkos aprašo V skyriuje nurodytas bazines kainas moka už žmogaus kraujodaros kamieninių ląstelių transplantacijos paslaugų atskirus etapus jas suteikusiai įstaigai, turinčiai licenciją teikti šias paslaugas ir sudariusiai sutartį su TLK dėl šių paslaugų teikimo ir jų išlaidų apmokėjimo.
19. Asmens sveikatos priežiūros įstaiga, kurios gydytojų konsiliumas priėmė sprendimą dėl transplantacijos atlikimo tikslingumo ir ją organizavo užsienyje, apmoka transplantaciją atlikusiai asmens sveikatos priežiūros įstaigai pagal faktines išlaidas, neviršydama jai skirtų asignavimų.
20. Pasibaigus ataskaitiniam mėnesiui, įstaiga, teikianti transplantacijos paslaugas, pateikia TLK sąskaitas ir statistinę ekonominę šių paslaugų teikimo ataskaitą Valstybinės ligonių kasos prie Sveikatos apsaugos ministerijos direktoriaus įsakymo nustatyta tvarka. TLK apmoka sąskaitas TLK ir įstaigos sutartyje numatyta tvarka, neviršydama Privalomojo sveikatos draudimo fondo biudžeto lėšų sumos, skirtos Transplantacijos programai vykdyti.
21. Viešajai sveikatos priežiūros įstaigai skirtos lėšos Transplantacijos programai finansuoti apskaitomos įstaigos banko atskiroje sąskaitoje.
V SKYRIUS
ŽMOGAUS KRAUJODAROS KAMIENINIŲ LĄSTELIŲ TRANSPLANTACIJOS PASLAUGŲ BAZINĖS KAINOS
22. Autologinė kraujodaros kamieninių ląstelių transplantacija
| Transplantacijos etapai |
I etapas: kamieninių ląstelių mobilizacijos, surinkimo (stacionare), užšaldymo ir laikymo išlaidos |
II etapas: pirmųjų 45 dienų AUTOKKLT (stacionare) išlaidos: recipiento kondicionavimas, kraujodaros kamieninių ląstelių infuzija į recipiento veną, pradinis laikotarpis po AUTOKKLT, kai būtina hospitalizuoti recipientą |
III etapas: AUTOKKLT (ambulatoriškai) išlaidos |
IV etapas: vėlyvųjų komplikacijų po AUTOKKLT, dėl kurių būtina recipientą hospitalizuoti, gydymo išlaidos |
| Bazinė kaina, balais (suaugusieji) |
8 269,97 |
36 116,45 |
1 859,52 |
34 267,04 |
| Bazinė kaina, balais (vaikai iki 18 metų) |
7 506,62 |
34 987,33 |
1 859,52 |
34 180,91 |
PASTABA. III etapas tęsiamas ir tada, kai pacientas hospitalizuojamas dėl nesusijusių su AUTOKKLT priežasčių. Susijusio su AUTOKKLT gydymo ir tyrimų išlaidos apmokamos iš Transplantacijos programos lėšų.
23. Alogeninė kraujodaros kamieninių ląstelių transplantacija
| Transplantacijos etapai |
I a etapas: giminingo donoro kraujodaros kamieninių ląstelių donacija |
I b etapas: negiminingo donoro (ND) paieška ir donacija |
II etapas: pirmųjų 100 dienų ALOKKLT (stacionare) išlaidos: recipiento kondicionavimas, donoro kraujodaros kamieninių ląstelių infuzija į recipiento veną, pradinis laikotarpis po ALOKKLT, kai reikia hospitalizuoti recipientą |
III etapas: ALOKKLT (ambulatoriškai) išlaidos |
IV etapas: vėlyvųjų komplikacijų po ALOKKLT, dėl kurių būtina recipientą hospitalizuoti, gydymo išlaidos |
| I b-1 etapas: ND paieška |
I b-2 etapas: ND kamieninių kraujodaros ląstelių donacija |
| Bazinė kaina, balais (suaugusieji) |
2 420,34 |
6 898,63 |
26 157,67 |
103 461,22 |
3 367,14 |
55 698,30 |
| Bazinė kaina, balais (vaikai iki 18 metų) |
2 420,34 |
6 898,63 |
26 157,67 |
103 410,29 |
3 367,14 |
53 831,67 |
PASTABOS:
a – vienos transplantacijos I b-1 ir I b-2 etapų kainos nustatomos: I b-1 etapo – už atliktą donoro paiešką (surastas recipientui tinkamas donoras arba donoro paieška nutraukta konsiliumo sprendimu, atlikus didelės skiriamosios gebos žmogaus leukocitų antigenų tipavimą); I b-2 etapo – už įvykdytą ND kamieninių kraujodaros ląstelių donaciją; į I b-1 etapo bazinę kainą įtrauktos šalies ir užsienio laboratorijose atliekamų vieno ND žmogaus leukocitų antigenų tipavimo tyrimų bei netiesioginės išlaidos; į I b-2 etapo bazinę kainą – ND kamieninių kraujodaros ląstelių surinkimo ir transportavimo paslaugų išlaidos;
b – III etapas tęsiamas ir tada, kai pacientas hospitalizuojamas dėl nesusijusių su ALOKKLT priežasčių. Susijusio su ALOKKLT gydymo ir tyrimų išlaidos apmokamos Žmogaus organų ir audinių transplantacijos paprastųjų išlaidų finansavimo programos lėšomis.
24. Vieno negiminingo donoro, įtraukto į Lietuvos negiminingų donorų registrą, tyrimo išlaidos – 308,49 euro.
_______________________
part_1353cb0863824ac89480f006dae6c149_end
Žmogaus kraujodaros kamieninių
ląstelių transplantacijos
paslaugų, apmokamų iš Transplantacijos
programos
lėšų, teikimo reikalavimų,
bazinių kainų ir mokėjimo
tvarkos aprašo
1 priedas

______________
part_2dbd0c1ac94045d9b14f52b1c3bd6a22_end
Žmogaus kraujodaros kamieninių
ląstelių transplantacijos
paslaugų, apmokamų iš Transplantacijos
programos
lėšų, teikimo reikalavimų,
bazinių kainų ir mokėjimo
tvarkos aprašo
2 priedas
Konsiliumo dėl indikacijų kraujodaros kamieninių ląstelių transplantacijai atlikti protokolas
Data …………………
Pacientui (-ei) …………………………………………………….……………….............................. ,
(vardas ir pavardė, asmens kodas)
sergančiam (-iai).................................................... ................................................................................,
(diagnozė)
neindikuotina / indikuotina atlikti …..................................................................................................... ........................................................... ………………....................................………………………….
(transplantacijos pavadinimas)
planinę / skubią kraujodaros kamieninių ląstelių transplantaciją.
Paciento (-ės) bendroji būklė pagal PSO: .............................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
................................................................................................................................................................
Konsiliumo dalyviai
1.................................................. ............................................................................................................
(vardas ir pavardė) (spaudas, parašas)
2................................................. .............................................................................................................
(vardas ir pavardė) (spaudas, parašas)
3.............................................. ................................................................................................................
(vardas ir pavardė) (spaudas, parašas)
......................................
(data)
Su konsiliumo išvadomis susipažinau:
.......................................................................................................................................... ......................
(paciento (paciento atstovo) vardas ir pavardė) (parašas)
......................................
(data)
______________
part_9322484b611649bd8d85bec4f32aaaa1_end
Žmogaus kraujodaros kamieninių
ląstelių transplantacijos
paslaugų, apmokamų iš Transplantacijos
programos
lėšų, teikimo reikalavimų,
bazinių kainų ir mokėjimo
tvarkos aprašo
3 priedas
ASMENS SUTIKIMAS, KAD JAM BŪTŲ ATLIKTA KRAUJODAROS KAMIENINIŲ LĄSTELIŲ TRANSPLANTACIJa
Aš,...................................... ........................................................................................................,
(vardas ir pavardė, asmens kodas)
gimęs (-usi)...................................... ..........................................................................................,
gyvenantis (-i)..................................... .......................................................................................,
esu informuotas (-a) apie mano ligos pobūdį, ištyrimą ir gydymą, susipažinau su Konsiliumo dėl indikacijų kraujodaros kamieninių ląstelių transplantacijai atlikti išvadomis. Man buvo išaiškinta ištyrimo ir gydymo rizika, galimos komplikacijos ir jų gydymo būdai.
Atlikus tyrimus buvo nustatyta, kad man reikalinga ši transplantacija.
Numatoma atlikti transplantacija:.......................................... ....................................................
Transplantacijos metu atsiradus nenumatytoms aplinkybėms, sutinku, kad medicinos personalas imtųsi visų būtinų priemonių ir procedūrų, kurios, jo nuomone, toje situacijoje bus būtinos.
Susipažinau su kiekvienos procedūros rizikos veiksniais. Esu nurodęs (-iusi) visas savo ankstesnes ligas, kurios gali turėti įtakos tyrimui ir gydymui. Mane taip pat informavo apie kitus galimus (alternatyvius) tyrimo ir gydymo metodus, jų privalumus, trūkumus, galimas komplikacijas ir gydymo sėkmę. Suprantu, kad medicinos praktikoje gali pasireikšti ir kitos su manimi neaptartos komplikacijos. Esu informuotas (-a), kad ligoninėje yra visos priemonės ir galimybės komplikacijas diagnozuoti ir gydyti. Patvirtinu, kad man nebuvo duota jokių besąlyginių pažadų ar garantijų dėl teigiamo procedūros rezultato ar baigties.
Man buvo suteikta visa su mano būkle susijusi informacija ir atsakyta į visus man kilusius klausimus. Daugiau klausimų neturiu.
Visa tai apsvarstęs (-iusi), pareiškiu savo sutikimą atlikti kraujodaros kamieninių ląstelių transplantaciją.
Pacientas ………….........………… Gydytojas ………………………………
(parašas) (spaudas, parašas)
Paciento atstovas ……………………......................……………….....................................................
(vardas ir pavardė, asmens kodas) (parašas)
.......... m............................. mėn. ...... d.
______________
part_a84332d7f63e4c669744fe6dccf67e5c_end
Žmogaus kraujodaros kamieninių
ląstelių transplantacijos
paslaugų, apmokamų iš Transplantacijos
programos
lėšų, teikimo reikalavimų,
bazinių kainų ir mokėjimo
tvarkos aprašo
4 priedas
asmens Sutikimas, kad jo kraujodaros kamieninės ląstelės būtų paimtos ir panaudotos transplantacijai
Aš,...................................... ........................................................................................................,
(vardas ir pavardė, asmens kodas)
gimęs (-usi)...................................... ..........................................................................................,
gyvenantis (-i)..................................... .......................................................................................,
esu informuotas (-a) apie kraujodaros kamieninių ląstelių paėmimo paskirtį, tikslus ir eigą. Man buvo išaiškinta šios procedūros rizika, galimos komplikacijos ir jų gydymo būdai.
Paėmimo metu atsiradus nenumatytoms aplinkybėms, sutinku, kad medicinos personalas imtųsi visų būtinų priemonių ir procedūrų, kurios, jo nuomone, toje situacijoje bus būtinos.
Man taip pat žinomas su kiekviena procedūra susijęs bendras rizikos veiksnys. Esu nurodęs (-iusi) visas savo ankstesnes ligas, kurios gali turėti įtakos tyrimui ir gydymui.
Suprantu, kad medicinos praktikoje gali pasireikšti ir kitos su manimi neaptartos komplikacijos. Esu informuotas (-a), kad ligoninėje yra visos priemonės ir galimybės komplikacijas diagnozuoti ir gydyti. Patvirtinu, kad man nebuvo duota jokių besąlyginių pažadų ar garantijų dėl teigiamo procedūros rezultato ar baigties.
Man buvo suteikta visa su mano būkle susijusi informacija ir atsakyta į visus man kilusius klausimus. Daugiau klausimų neturiu.
Visa tai apsvarstęs (-iusi), reiškiu savo sutikimą man atlikti kraujodaros kamieninių ląstelių donavimo procedūrą.
Donoras ………….........………… Gydytojas ………………………………
(parašas) (spaudas, parašas)
Donoro (paciento) atstovas ……………………......................………………......................................
(vardas ir pavardė, asmens kodas) (parašas)
.......... m............................. mėn. ...... d.
______________
part_467255daf248438a8b30ecf4294af172_end
Žmogaus kraujodaros kamieninių
ląstelių transplantacijos
paslaugų, apmokamų iš Transplantacijos
programos lėšų, teikimo reikalavimų,
bazinių kainų ir mokėjimo
tvarkos aprašo
5 priedas
DONORO ir (AR) recipiento IŠTYRIMas prieš kraujodaros kamieninių ląstelių transplantaciją
1. Klinikinis tyrimas:
1.2. burnos ir akių gleivinės apžiūra;
1.4. limfmazgių palpacija;
1.5. arterinio kraujospūdžio matavimas;
1.6. temperatūros matavimas;
1.7. pulso dažnio matavimas;
1.8. krūtines ląstos organų auskultacija;
1.9. pilvo ertmės organų palpacija;
1.10. periferinių venų būklės įvertinimas.
2. Instrumentinis tyrimas:
2.2. tiesinė krūtinės ląstos rentgenograma.
3. Laboratorinis tyrimas:
3.1. bendras kraujo tyrimas;
3.2. bendras šlapimo tyrimas;
3.3. kaulų čiulpų aspiracinė biopsija (jei yra medicininių indikacijų);
3.4. kraujo ABO grupė, Rh faktorius;
3.6. alanininė transaminazė;
3.7. asparaginininė transaminazė;
3.15. hepatito B viruso paviršinis antigenas (HBsAg);
3.16. hepatito B viruso šerdinio antigeno antikūnai (anti-HBc);
3.17. hepatito C viruso antikūnai (anti-HCV);
3.18. žmogaus imunodeficito viruso ŽIV-I ir ŽIV-II antikūnai (anti-ŽIV-I/II);
3.19. citomegalijos viruso IgG ir IgM antikūnai (Anti-CMV IgG ir IgM);
3.20. sifilio serologinis tyrimas.
__________________________
part_1e7e1fec2e8c465b843c662e9f710376_end
Žmogaus kraujodaros kamieninių
ląstelių transplantacijos
paslaugų, apmokamų iš Transplantacijos
programos
lėšų, teikimo reikalavimų,
bazinių kainų ir mokėjimo
tvarkos aprašo
6 priedas
DONORO, kurį ketinama įtraukti į lietuvos negiminingų donorų registrą, ištyrimas
1. Žmogaus leukocitų antigenų (ŽLA) I klasės tyrimas.
2. ŽLA II klasės tyrimas.
part_622819712f9e4e1286911f7f71719d9c_end
Žmogaus kraujodaros kamieninių
ląstelių transplantacijos
paslaugų, apmokamų iš Transplantacijos
programoslėšų, teikimo reikalavimų,
bazinių kainų ir mokėjimo
tvarkos aprašo
7 priedas
Negiminingo kraujodaros kamieninių ląstelių potencialaus donoro anketa
Prašome atidžiai užpildyti šią anketą. Jūsų atsakymai yra konfidencialūs. Tikslūs atsakymai į pateiktus klausimus svarbūs tam, kad būtų apsaugota Jūsų sveikata ir kad būtų apsaugotas pacientas, kuriam bus persodintos Jūsų kraujodaros kamieninės ląstelės. Pažymėkite tinkamus atsakymus – taip arba ne.
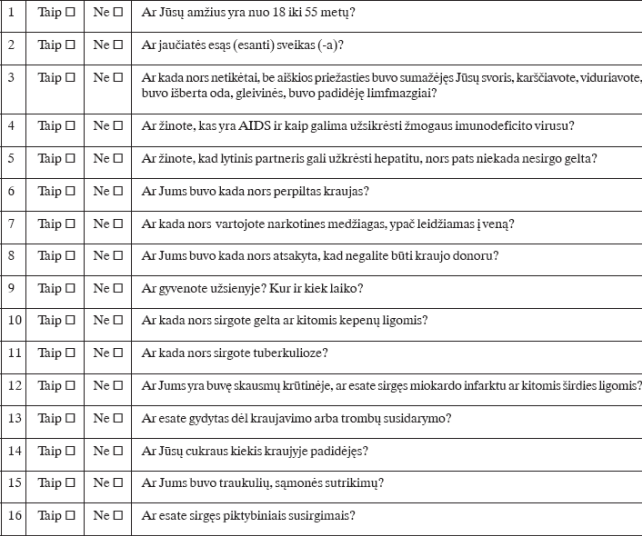
Prašome paaiškinti, jeigu į kuriuos nors klausimus, išskyrus 1, 2, 4 ir 5, atsakėte „taip“.
______________
part_542257dcbfd94ac09c73968abad55b30_end
Žmogaus kraujodaros kamieninių
ląstelių transplantacijos
paslaugų, apmokamų iš Transplantacijos
programos
lėšų, teikimo reikalavimų,
bazinių kainų ir mokėjimo
tvarkos aprašo
8 priedas
asmens sutikimas, kad jo duomenys būtų UŽregistruoti lietuvos negiminingų donorų registre
Sveikatos priežiūros įstaiga..................................................... ...................................................
(pavadinimas, kodas)
Aš,......................................................... .....................................................................................,
(vardas ir pavardė, asmens kodas)
................................................................................................................................................... ,
(telefonai, adresai)
sutinku, kad mano duomenys būtų įtraukti į Lietuvos negiminingų donorų registrą. Esu informuotas (-a) apie registro sudarymo tikslą, susipažinęs (-usi) su galima rizika, taip pat žinau, kad tapęs (-usi) savanoriu donoru negaliu tikėtis atlygio / užmokesčio.
Esu informuotas (-a), kad bet kada galiu atsisakyti šio sutikimo apie tai raštu pranešęs (-usi) Lietuvos negiminingų donorų registro tvarkytojui.
Pareiškiu, kad mano veiksnumas nėra ribotas.
Data............................................................................................................................................ .
Asmens parašas..........................................................................................................................
Informavusio gydytojo parašas, spaudas....................................................................................
______________
part_3599108360254e81b7cb2dcee9cef14c_end
![]()

